
| A. | Y、Z、W的简单离子半径Z>W>Y | B. | 工业上制取Y可用电解YW3制得 | ||
| C. | XW2中各原子均达到8电子结构 | D. | Z、W的氧化物对应水化物的酸性Z<W |
分析 X、Y、Z、W是原子序数依次增大的不同主族短周期元素,其中两种为金属元素,X原子的最外层电子数与次外层电子数相等,则X只能含有2个电子层,最外层含有2个电子,为Be元素;X与W的最外层电子数之和为9,W的最外层电子数为:9-2=7,为ⅤⅡA族元素;Y与Z的最外层电子数之和为9,五种元素均不同主族,则Y、Z的最外层电子数为3、6或4、5,再结合“其中两种为金属元素”可知Y、Z的最外层电子数只能为3、6,且Y为Al、Z为S元素,结合原子序数大小可知W为Cl元素,据此进行解答.
解答 解:A.Y为Al、Z为S、W为Cl元素,铝离子含有2个电子层,硫离子、氯离子含有3个电子层,则铝离子的离子半径最小,S元素的核电荷数较小,则硫离子的离子半径大于氯离子,所以Y、Z、W的简单离子半径大小为:Z>W>Y,故A正确;
B.Y为Al,YW3为AlCl3,氯化铝而为共价化合物,熔融氯化铝不导电,工业上通过电解氧化铝获得铝,故B错误;
C.XW2为BeCl2,Be原子不满足8电子稳定结构,故C错误;
D.“Z、W的最高价氧化物对应水化物的酸性:Z<W”没有指出最高价,该说法不一定成立,故D错误;
故选A.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意限制条件“其中两种为金属元素”,试题培养了学生的分析能力及灵活应用能力.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:选择题
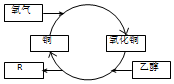
| A. | R的化学式为C2H4O | |
| B. | 乙醇发生了还原反应 | |
| C. | 反应过程中固体有红黑交替变化的现象 | |
| D. | 乙二醇(HO-CH2-CH2-OH)也能发生类似反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
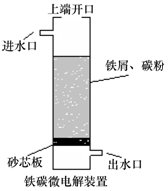
| A. | 无论是否鼓入空气,负极的电极反应式均为Fe-2e-═Fe2+ | |
| B. | 不鼓入空气时,正极的电极反应式为H++e-═H | |
| C. | 鼓入空气时,每生成1mol•OH有2mol电子发生转移 | |
| D. | 处理含有草酸(H2C2O4)的污水时,上端开口应打开并鼓入空气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 200 | 300 | 400 |
| K | 290 | 39 | 11.7 |
| 实验Ⅰ | 实验Ⅱ | |
| 通入气体 | CO、H2 | CO、H2、H2O(g) |
| 固体产物 | Fe3O4、Fe | Fe3O4 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-+H2O?H3O++CO32- | B. | HS-+H2O?H2S+OH- | ||
| C. | HSO3-+H2O?SO32-+H3O+ | D. | HCO3-+OH-?H2O+CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com