
Ζ÷Έω Θ®1Θ©ΗυΨί≈δ÷Τ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»»ή“Κ”ΟΒΫ“«Τς―Γ‘ώΘΜΗυΨί≈δ÷Τ»ή“ΚΒΡΧεΜΐ―Γ‘ώ»ίΝΩΤΩΒΡΙφΗώΘΜ
Θ®2Θ©»ίΝΩΤΩ≤ΜΡήœΓ Ά≈®»ή“ΚΓΔ≤ΜΡή”Ο”Ύ»ήΫβΙΧΧεΓΔ¥Δ¥φ»ή“ΚΒ»Θ§ «≈δ÷Τ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»»ή“ΚΒΡΉ®”Ο“«ΤςΘΜ
Θ®3Θ©Ζ÷Έω≤ΌΉςΕ‘»ή÷ ΒΡΈο÷ ΒΡΝΩΚΆ»ή“ΚΧεΜΐΒΡ”ΑœλΘ§“άΨίC=$\frac{n}{V}$Ϋχ––Έσ≤νΖ÷ΈωΘΜ
Θ®4Θ©ΗυΨίc=$\frac{1000Π―ΠΊ}{M}$ΦΤΥψ≥ωΗΟ≈®ΝρΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»Θ§‘ΌΗυΨί≈δ÷ΤΙΐ≥Χ÷–»ή÷ ΝρΥαΒΡΈο÷ ΒΡΝΩ≤Μ±δΦΤΥψ≥ω–η“Σ≈®ΝρΥαΒΡΧεΜΐΘΜ“άΨί≈®ΝρΥαœΓ ΆΒΡ’ΐ»Ζ≤ΌΉςΫβ¥πΘ°
Ϋβ¥π ΫβΘΚΘ®1Θ©≈δ÷Τ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»»ή“Κ”ΟΒΡ“«Τς”–ΘΚΆ–≈ΧΧλΤΫΓΔ“©≥ΉΓΔ…’±≠ΓΔΆ≤ΝΩΓΔ≤ΘΝßΑτΓΔ»ίΝΩΤΩΓΔΫΚΆΖΒΈΙήΘ§≤Μ–η“ΣΒΡ“«Τς”–…’ΤΩΚΆΖ÷“Κ¬©ΕΖΘ§“Σ≈δ÷Ο450ml»ή“Κ”Π―Γ‘ώ500ml»ίΝΩΤΩΘΜΜΙ»±…ΌΒΡ“«ΤςΘΚ…’±≠ΓΔ≤ΘΝßΑτΘΜ
Ι ¥πΑΗΈΣΘΚAΓΔCΘΜ …’±≠ΓΔ≤ΘΝßΑτΘΜ
Θ®2Θ©»ίΝΩΤΩ÷ΜΡή”Οά¥≈δ÷Τ“ΜΕ®ΧεΜΐΉΦ»Ζ≈®Ε»ΒΡ»ή“ΚΘ§≤ΜΡή≈δ÷ΤΜρ≤βΝΩ»ίΝΩΤΩΙφΗώ“‘œ¬ΒΡ»Έ“βΧεΜΐΒΡ“ΚΧεΘ§≤ΜΡήœΓ ΆΜρ»ήΫβ“©ΤΖΘ§≤ΜΡή”Οά¥Φ”»»»ήΫβΙΧΧε»ή÷ Θ§Ι ―ΓBCEΘΜ
Ι ¥πΑΗΈΣΘΚBCEΘΜ
Θ®3Θ©‘Ύ Β―ι÷–ΤδΥϊ≤ΌΉςΨυ’ΐ»ΖΘ§»τΕ®»ί ±―ω ”ΩΧΕ»œΏΘ§ΒΦ÷¬»ή“ΚΧεΜΐΤΪ¥σΘ§»ή“Κ≈®Ε»ΤΪ–ΓΘΜ
»τNaOH»ή“Κ‘ΎΉΣ“Τ÷Ν»ίΝΩΤΩ ±Έ¥Ψ≠ά以ȧά以ΚσΘ§»ή“ΚΧεΜΐΤΪ–ΓΘ§»ή“Κ≈®Ε»ΤΪ¥σΘΜ
Ι ¥πΑΗΈΣΘΚ–Γ”ΎΘΜ¥σ”ΎΘΜ
Θ®4Θ©Ζ÷ ΐΈΣ98%ΓΔΟήΕ»ΈΣ1.84g•cm-3ΒΡ≈®ΝρΥαΒΡ≈®Ε»ΈΣΘΚc=$\frac{1000ΓΝ1.84ΓΝ98%}{98}$mol/L=18.4mol/LΘ§
≈δ÷ΤΙΐ≥Χ÷–ΝρΥαΒΡΈο÷ ΒΡΝΩ≤Μ±δΘ§‘ρ–η“ΣΗΟ≈®ΝρΥαΒΡΧεΜΐΈΣΘΚ$\frac{0.5mol/LΓΝ0.5L}{18.4mol/L}$=13.6mLΘΜ
≈®ΝρΥαœΓ ΆΒΡ’ΐ»Ζ≤ΌΉςΘΚΫΪ≈®ΝρΥα―ΊΤς±ΎΜΚΜΚΒΙ»κΥ°÷–Θ§≤Δ”Ο≤ΘΝßΑτ≤ΜΕœΫΝΑηΘΜ
Ι ¥πΑΗΈΣΘΚ13.6ΘΜΫΪ≈®ΝρΥα―ΊΤς±ΎΜΚΜΚΒΙ»κΥ°÷–Θ§≤Δ”Ο≤ΘΝßΑτ≤ΜΕœΫΝΑηΘ°
ΒψΤά ±ΨΧβΩΦ≤ιΝΥΈο÷ ΒΡΝΩ≈®Ε»ΒΡΦΤΥψΘ§ΧβΡΩΡ―Ε»÷–Β»Θ§Ος»ΖΈο÷ ΒΡΝΩ≈®Ε»”κ»ή÷ ÷ ΝΩΖ÷ ΐΒΡΙΊœΒΈΣΫβ¥πΙΊΦϋΘ§ΉΔ“β’ΤΈ’œΓ ΆΕ®¬…‘ΎΜ·―ßΦΤΥψ÷–ΒΡ”Π”ΟΖΫΖ®Θ§ ‘Χβ≈ύ―χΝΥ―ß…ζΒΡΜ·―ßΦΤΥψΡήΝΠΘ°


 Ϋρ«≈ΫΧ”ΐΦΤΥψ–ΓΉ¥‘ΣœΒΝ–¥πΑΗ
Ϋρ«≈ΫΧ”ΐΦΤΥψ–ΓΉ¥‘ΣœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | ΒΞ÷ Ιη”Ο”Ύ÷Τ‘λ–ΨΤ§ΚΆΙβΒΦœΥΈ§ | |
| BΘ° | 84œϊΕΨ“ΚΒΡ”––ß≥…Ζ÷ «NaClO | |
| CΘ° | SO2ΨΏ”–Τ·ΑΉ–‘Θ§Ά®»κΉœ…Ϊ ·»ο»ή“Κ÷–Ρή Ι»ή“Κœ»±δΚλΚσΆ …Ϊ | |
| DΘ° | Τ’Ά®≤ΘΝßΒΡΉι≥…Ω…”ΟNa2O•CaO•6SiO2±μ ΨΘ§ «¥ΩΨΜΈο |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | cΘ®H+Θ© | BΘ° | KbΘ®NH3•H2OΘ© | ||
| CΘ° | $\frac{cΘ®N{H}_{3}•{H}_{2}OΘ©}{cΘ®N{{H}_{4}}^{+}Θ©}$ | DΘ° | cΘ®NH4+Θ© |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ

| AΘ° | ‘≠Ή” | BΘ° | Ζ÷Ή” | CΘ° | ΒΞ÷ | DΘ° | ‘ΣΥΊ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
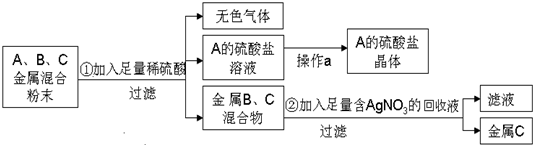
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com