
【题目】草酸是草本植物常具有的成分。查阅相关资料得到草酸晶体(H2C2O4·3H2O)及其盐的性质如下表。

(1)草酸晶体(H2C2O4·3H2O)175℃以上会发生分解生成三种氧化物,某实验小组欲通过实验证明这三种氧化物。
①该小组选用装置丙作为分解装置,不选用甲装置的原因是________________。丙装置相对于乙装置的优点是____________。实验前检验该装置气密性的操作方法是_________。
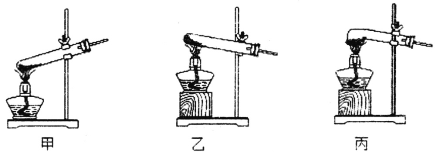
②从下图选用合适的装置,验证分解产生的气体,装置的连接顺序是____________。(用装置编号表示,某些装置可以重复使用,也可以装不同的试剂)
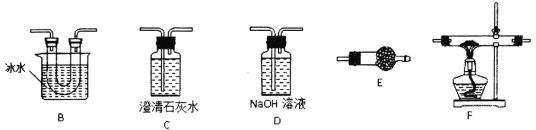
③B装置的作用是________________________。
(2)某实验小组称取4.0g粗草酸晶体配成100mL溶液,采用0.1mol·L-1酸性高锰酸钾溶液滴定该草酸溶液,测定该草酸晶体的纯度。
①配制草酸溶液需要用到的主要玻璃仪器有_______________。
②本实验达到滴定终点的标志是______________________。
③将所配草酸分为四等份,实验测得每份平均消耗酸性高锰酸钾溶液20mL。计算该粗草酸中含草酸晶体的质量为_______g(保留两位有效数字)。
【答案】甲装置管口向上,反应时生成的水蒸气冷凝回流易使试管炸裂 乙装置直接管口向下,晶体熔化成液态后会流出试管,而丙装置会避免这种情况发生 将丙装置导气管插入水中,加热,若导气管冒气泡,撤灯后回流一段水柱,证明装置气密性良好 EBCDCEFC 冷凝草酸,防止生成白色草酸钙沉淀干扰CO2的检验 烧杯、玻璃棒、容量瓶、胶头滴管(可写可不写) 最后一滴高锰酸钾滴入,溶液突然无色变到粉红色(或淡红色)且半分钟内颜色不变 2.9
【解析】
(1)①该小组选用装置丙作为分解装置,不选用甲装置的原因是甲装置管口向上,反应时生成的水蒸气冷凝回流易使试管炸裂。丙装置相对于乙装置的优点是乙装置直接管口向下,晶体熔化成液态后会流出试管,而丙装置会避免这种情况发生。根据热胀冷缩的原理,实验前检验该装置气密性的操作方法是将丙装置导气管插入水中,加热,若导气管冒气泡,撤灯后回流一段水柱,证明装置气密性良好。
故答案为:甲装置管口向上,反应时生成的水蒸气冷凝回流易使试管炸裂;乙装置直接管口向下,晶体熔化成液态后会流出试管,而丙装置会避免这种情况发生;将丙装置导气管插入水中,加热,若导气管冒气泡,撤灯后回流一段水柱,证明装置气密性良好;
②草酸晶体分解生成二氧化碳、一氧化碳、水,通过E验证分解产生的气体中含水,再通过B装置,冷凝草酸,防止生成白色草酸钙沉淀干扰,用C检验产生的CO2,用D除去CO2,用C检验CO2是否除尽,将余下的气体通过F,用CuO与余下的气体反应,两用C检验生成的气体,装置的连接顺序是EBCDCEFC。故答案为:EBCDCEFC;

③B装置的作用是冷凝草酸,防止生成白色草酸钙沉淀干扰,故答案为:冷凝草酸,防止生成白色草酸钙沉淀干扰;
(2)某实验小组称取4.0g粗草酸晶体配成100mL溶液,采用0.1mol·L-1酸性高锰酸钾溶液滴定该草酸溶液,测定该草酸晶体的纯度。
①配制草酸溶液需要用到的主要玻璃仪器有:烧杯、玻璃棒、100mL容量瓶、胶头滴管(可写可不写)。故答案为:烧杯、玻璃棒、100mL容量瓶、胶头滴管;
②本实验达到滴定终点的标志是:滴入最后一滴溶液变为紫红色且半分钟不褪色证明反应达到终点,
故答案为:当滴下最后一滴KMnO4溶液,溶液由无色变浅红色,且半分钟内不变色;
③将所配草酸分为四等份,实验测得每份平均消耗酸性高锰酸钾溶液20mL。
滴定时酸性的KMnO4溶液能氧化H2C2O4,生成CO2气体,同时本身被还原为Mn2+,发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O,可得关系式:5H2C2O4·3H2O~2MnO4-,m(H2C2O4·3H2O)=![]() =2.9g;故答案为:2.9g。
=2.9g;故答案为:2.9g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】分析如图所示的四个原电池装置,其中结论正确的是
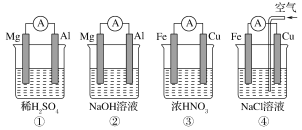
A. ①②中Mg作负极,③④中Fe作负极
B. ②中Mg作正极,正极反应式为6H2O+6e-==6OH-+3H2↑
C. ③中Fe作负极,电极反应式为Fe-2e-==Fe2+
D. ④中Cu作正极,电极反应式为2H++2e-==H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,某科研小组设计如下工艺流程回收铜并制取胆矾(流程中RH为萃取剂),下列说法正确的是

A.反应I的离子方程式为:Cu+H2O+2NH3+2NH4+==Cu(NH3)42++2H2O
B.操作②用到的主要仪器为蒸馏烧瓶
C.操作④以石墨为电极电解硫酸铜溶液:阳极产物为O2和H2SO4
D.操作⑤为:蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的恒容容器中,能标志某可逆反应2A(g)+2B(g)![]() C(g)+3D(g)己达平衡状态的是
C(g)+3D(g)己达平衡状态的是
A.混合气体的密度保持不变B.气体A的质量不随时间变化而变化
C.2v正(A)=3v逆(D)D.混合气体的压强不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
反应1:Fe2O3(s)+3C(石墨,s) ![]() 2Fe(s)+3CO(g) △H 1
2Fe(s)+3CO(g) △H 1
反应2:C(石墨,s)+CO2(g)![]() 2CO(g) △H 2
2CO(g) △H 2
①△H=__(用含△H1、△H2代数式表示)
②保持温度不变,在恒容容器中进行反应1,达到平衡状态,再次充入一定量的CO(Fe足量),则平衡__移动(填“正向”或“逆向”),达到新平衡后c(CO)将__(填“变大”、“变小”或“不变”)
(2)氯化铵常用作除锈剂,其水溶液呈酸性的原因是__。
(3)硫酸铝水解的离子方程式是__,为了抑制其水解,配制时可以加入少量的__。
(4)泡沫灭火器中装的灭火剂主要包括硫酸铝溶液、碳酸氢钠溶液。泡沫灭火器内置的玻璃筒应装__溶液,外部的铁筒装另一种溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.标准状况下0.5molNT3分子中所含中子数为6.5NA
B.0.1molFe与0.1molCl2完全反应后,转移的电子数为0.2NA
C.13.35gAlCl3水解形成的Al(OH)3胶体粒子数小于0.1NA
D.一定条件下的密闭容器中,2molSO2和1molO2催化反应充分发生后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4+6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察____________________。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______色变成____________色。
(2)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品中氮的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物分别溶于水得溶液,0.010mol/L的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是( )

A.Y可能是硅元素
B.简单离子半径:Z>W>X
C.气态氢化物的稳定性:Y>W
D.非金属性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A在一定条件下可发生如图转化。
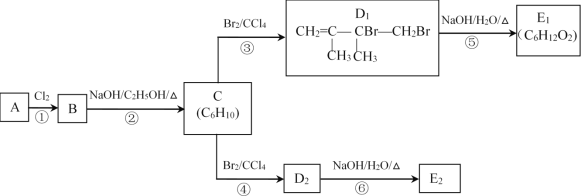
已知:A的质谱图表明其相对分子质量为84,其核磁共振氢谱只有一种氢。E1、E2互为同分异构体。
(1)D1是否存在顺反异构___(填“是”或“否”)。
(2)①至⑥的反应中,属于加成反应的是___。
(3)C的化学名称是___。
(4)写出A在一定条件下发生加聚反应的化学方程式___。
(5)E2的结构简式为___。
(6)写出反应②的化学方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com