
£Ø10·Ö£©Ä³»ÆѧĢ½¾æѧĻ°Š”×éĶ¬Ń§ŌŚŹµŃéŹŅÖŠÅäÖĘ100mL 0.5mol/LµÄNa2CO3ČÜŅŗ”£
£Ø1£©ĻĀĮŠŹµŃé²½ÖčŹĒÅäÖĘČÜŅŗĖł±ŲŠčµÄ²½Öč£¬ĒėŹ¹ÓĆø÷²½ÖčµÄ±ąŗÅ°“ÕÕŹµŃé²Ł×÷Ź±µÄĖ³Šņ½ųŠŠÅÅŠņ(ĢīŠ“ø÷²½ÖčµÄ±ąŗÅ)_______________________£»
¢ŁČܽā ¢Ś¶ØČŻ ¢Ū¼ĘĖć ¢Ü×ŖŅĘ ¢Ż³ĘĮæ ¢ŽĻ“µÓ²¢×ŖŅĘ ¢ß·“ø“µ¹×ŖŅ”ŌČ
£Ø2£©ŹµŃéÖŠ³żĮĖŠčŅŖĢģĘ½”¢Ņ©³×”¢ÉÕ±”¢²£Į§°ōĶā£¬»¹ŠčŅŖµÄŅĒĘ÷ÓŠ_______________£»
£Ø3£©ÓĆĢ¼ĖįÄĘ¾§Ģå£ØNa2CO3”¤10H2O£©ÅäÖĘøĆČÜŅŗŠčŅŖ g£¬Čō³ĘČ”µČÖŹĮæµÄNa2CO3 £¬ŌņĖłÅäÖĘČÜŅŗµÄÅØ¶Č £ØĢīŠ“Ę«øß”¢Ę«µĶ”¢ĪŽÓ°Ļģ£©£»
£Ø4£©øĆŠ”×éŌŚŹµŃéŹŅÖŠ·¢ĻÖĮĖŅ»ÕÅ×¢ÉäÓĆÖŹĮæ·ÖŹżĪŖ5%µÄĘĻĢŃĢĒ(·Ö×ÓŹ½ĪŖC6H12O6£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ180)ČÜŅŗµÄ±źĒ©£¬ČēĻĀĶ¼ĖłŹ¾£ŗ

øĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ________(Š”Źżµćŗó±£Įō2Ī»Źż)”£
£Ø1£©¢Ū¢Ż¢Ł¢Ü¢Ž¢Ś¢ß£» £Ø2£©100mLČŻĮæĘ攢½ŗĶ·µĪ¹Ü£» £Ø3£©14.3£¬Ę«øߣ»£Ø4£©0.28 mol”¤L-1
”¾½āĪö”æ
ŹŌĢā½āĪö£ŗ£Ø1£©¹ĢĢåÅäÖĘČÜŅŗµÄŅ»°ć²½ÖčĪŖ¼ĘĖć”¢³ĘĮ攢Čܽā”¢×ŖŅĘ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČ£¬¹ŹÕżČ·Ė³ŠņĪŖ£ŗ¢Ū¢Ż¢Ł¢Ü¢Ž¢Ś¢ß£»
£Ø2£©ÅäÖĘ100mL 0.5mol?L-1µÄNaClČÜŅŗ£¬ĖłŅŌ»¹ŠčŅŖ500mlČŻĮæĘ棬ČܽāŠčŅŖÓĆÉÕ±”¢²£Į§°ō£¬²£Į§°ō½Į°č£¬¼ÓĖŁČܽā£»×ŖŅĘŠčŅŖ²£Į§°ōŅżĮ÷£»¶ØČŻŠčŅŖÓĆ100mlČŻĮæĘæŗĶ½ŗĶ·µĪ¹Ü£¬¹Ź»¹ŠčŅŖµÄŅĒĘ÷ŹĒ100mLČŻĮæĘ攢½ŗĶ·µĪ¹Ü£»
£Ø3£©n=cV=0.1L”Į0.5mol/L=0.05mol£¬m=nM=286g/mol”Į0.05mol=14.3g£»Čō³ĘČ”µČÖŹĮæµÄNa2CO3 £¬ŌņČÜÖŹµÄĪļÖŹµÄĮæĘ«“ó£¬ĖłÅäÖĘČÜŅŗµÄÅضČĘ«øߣ»£Ø4£©ÓɱźĒ©æÉÖŖ£¬500mLČÜŅŗÖŠŗ¬ÓŠĘĻĢŃĢĒ25g£¬ĘĻĢŃĢĒµÄÖŹĮæ=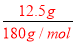 =
=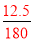 moll£¬¹ŹĘĻĢŃĢĒµÄĪļÖŹµÄĮæÅضČ=
moll£¬¹ŹĘĻĢŃĢĒµÄĪļÖŹµÄĮæÅضČ=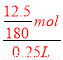 =0.28mol/L”£
=0.28mol/Lӣ
æ¼µć£ŗŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗµÄÅäÖĘ”¢ĪļÖŹµÄĮæÅØ¶ČµÄ¼ĘĖć



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢ĮņĖįŠĶĖįÓźµÄŠĪ³É»įÉę¼°·“Ó¦£ŗ2H2SO3+O2
| ||||
| B”¢Ć÷·Æ·ÅČėĖ®ÖŠæÉŠĪ³É“ųÕżµēµÄAl£ØOH£©3½ŗĮ££ŗAl3++3H2O?Al£ØOH£©3£Ø½ŗĢ壩+3H+ | ||||
| C”¢Ń”ÓĆCuSO4ČÜŅŗ³żČ„ŅŅČ²ĘųĢåÖŠµÄH2S£ŗH2S+Cu2+ØTCuS”ż+2H+ | ||||
| D”¢Čȵēæ¼īŅŗæÉŅŌĒåĻ“ÓĶĪŪµÄŌŅņ£ŗCO32?+2H2O?H2CO3+2OH? |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ¹ć¶«Ź”ÉŲ¹ŲŹŠŹ®Š£øßČż10ŌĀĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
(16·Ö)ŌŚŅ»¶ØĢõ¼žĻĀ£¬NOÓėNO2»ģŗĻæÉÉś³ÉN2O3 £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
NO£Øg£©+NO2£Øg£© N2O3£Øl£© ”÷H£¼0
N2O3£Øl£© ”÷H£¼0
ĻĀĶ¼±ķŹ¾Ņ»¶ØĮæµÄNO”¢NO2»ģŗĻĘųĢå·¢Éś·“Ó¦Ź±£¬N02ÅضČŌŚĒ°25sÄŚµÄ±ä»Æ”£øĆ·“Ó¦½ųŠŠµ½45sŹ±“ļµ½Ę½ŗā£¬²āµĆNO2ÅضČŌ¼ĪŖ0.010mol/L”£

£Ø1£©Ē°20sÄŚ,NO2µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_________________”£
£Ø2£©ĘäĖūĢõ¼ž²»±ä£¬¢ŁÉżøßĪĀ¶Č£¬NO2µÄ×Ŗ»ÆĀŹ_______ (Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
¢ŚŃ¹ĖõĘųĢåĢå»ż£¬øĆ·“Ó¦Ę½ŗāĻņ______ _ŅʶÆ(Ģī”°ÕżĻņ”±»ņ”°ÄęĻņ”±)”£
£Ø3£©Čō·“Ó¦ŃÓŠųÖĮ70Ćė£¬ĒėŌŚ“šĢāæØĶ¼ÖŠ»³ö25ĆėÖĮ70ĆėµÄ·“Ó¦½ų³ĢĒśĻß”£
£Ø4£©ČōŌŚ·“Ó¦æŖŹ¼Ź±¼ÓČė“߻ƼĮ(ĘäĖūĢõ¼ž¶¼²»±ä)£¬ĒėŌŚ“šĢāæØĶ¼ÖŠ»³ö¼Ó“߻ƼĮŗóµÄ·“Ó¦½ų³ĢĒśĻß”£
£Ø5£©NO”¢NO2µÄ»ģŗĻĘųĢåÓĆNaOHČÜŅŗĪüŹÕ£¬µĆµ½µÄŃĪÖ»ÓŠŅ»ÖÖ£¬ŌņøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ______£¬øĆ·“Ó¦µÄŃõ»Æ¼ĮŹĒ______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ¹ć¶«Ź”Õæ½ŹŠøßČżµŚŅ»“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ·ÖĄė”¢Ģį“攢¼ų±šĪļÖŹµÄ·½·ØÕżČ·µÄŹĒ
A£® Óƶ”“ļ¶ūŠ§Ó¦¼ų±šFe(OH)3½ŗĢåŗĶFeCl3ČÜŅŗ
B£® ÓĆ¹żĀĖµÄ·½·Ø³żČ„NaClČÜŅŗÖŠŗ¬ÓŠµÄÉŁĮæµķ·Ū½ŗĢå
C£® ÓĆČܽā”¢¹żĀĖµÄ·½·ØĢį“æŗ¬ÓŠÉŁĮæBaSO4µÄBaCO3
D£® ÓĆ¼ÓČČ”¢Õō·¢µÄ·½·ØæÉŅŌ³żČ„“ÖŃĪÖŠµÄCaCl2”¢MgCl2µČŌÓÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ¹ć¶«Ź”Õæ½ŹŠøßŅ»µŚŅ»Ń§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Š”Ć÷¼ŅÖŠÓŠČēĻĀÉś»īÓĆĘ·£ŗµā¾Ę”¢Ź³ŃĪ”¢Ź³“×”¢84Ļū¶¾Ņŗ£ØÓŠŠ§³É·ÖĪŖNaClO£©£¬Š”Ć÷ĄūÓĆÉĻŹöÓĆĘ·²»ÄÜĶź³ÉµÄČĪĪńŹĒ
A£®¼ģŃéĀņĄ“µÄÄĢ·ŪÖŠŹĒ·ń¼ÓÓŠµķ·Ū
B£®¼ģŃé×ŌĄ“Ė®ÖŠŹĒ·ńŗ¬ÓŠCl£
C£®³żČ„±£ĪĀĘæÖŠµÄĖ®¹ø
D£®Ļ“Č„°×É«ŅĀ·žÉĻµÄ·¬ĒŃÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½ĖÕŹ”ŃĪ³ĒŹŠ”¢½Øŗž¶žÖŠøßŅ»ÉĻѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÅäÖĘŅ»¶ØĢå»ż£¬Ņ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗŹ±£¬ĻĀĮŠĒéæöÖŠČÜŅŗµÄÅضČĘ«Š”µÄŹĒ
A”¢Čܽāŗó£¬ČÜŅŗĪ“¾ĄäČ“£¬Į¢¼“×ŖŅĘÖĮČŻĮæĘæ
B”¢½ŗĶ·µĪ¹ÜµĪ¼ÓÕōĮóĖ®Ź±£¬²»Š”ŠÄ°ŃÉŁĮæµÄÕōĮóĖ®µĪµ½ČŻĮæĘæĶā
C”¢×ŖŅĘČÜŅŗŗó£¬Ī“Ļ“µÓÉÕ±ŗĶ²£Į§°ō¾ĶÖ±½Ó¶ØČŻ
D”¢¶ØČŻŹ±£¬ø©ŹÓæĢ¶ČĻß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½ĖÕŹ”ŃĪ³ĒŹŠ”¢½Øŗž¶žÖŠøßŅ»ÉĻѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ0.5 LČÜŅŗÖŠŗ¬ÓŠ0.1 mol NaClŗĶ0.2 mol MgCl2£¬Ōņ“ĖČÜŅŗÖŠĀČĄė×ÓµÄĪļÖŹµÄĮæÅØ¶ČŹĒ
A”¢0.3 mol”¤L£1 B”¢0.5 mol”¤L£1
C”¢0.6 mol”¤L£1 D”¢1 mol”¤L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½ĖÕŹ”»“°²ŹŠøßČżÉĻѧʌµŚŅ»“Ī½×¶ĪŠŌ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ijĀĮĶĮæóÖŠÖ÷ŅŖŗ¬ÓŠAl2O3”¢Al(OH)3”¢AlO(OH)£¬»¹ŗ¬ÓŠFe2O3µČŌÓÖŹ”£ĄūÓĆ°Ż¶ś·ØÉś²śŃõ»ÆĀĮµÄĮ÷³ĢČēĻĀĶ¼ĖłŹ¾£ŗ

£Ø1£©¼ī½žŹ±ĪŖĢįøßĀĮĶĮæóµÄ½ž³öĀŹæɲÉČ”µÄ“ėŹ©ŹĒ £¬ ”££Ø“šĮ½µć£©
£Ø2£©AlO(OH)ÓėNaOH·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©ŌŚĻ”ŹĶ”¢½į¾§¹ż³ĢÖŠ,¼ÓAl(OH)3¾§ŗĖµÄÄæµÄŹĒ“Ł½ųAl(OH)3µÄĪö³ö”£ÉĻŹö”°Ļ”ŹĶ”¢½į¾§”±¹¤ŅÕ£¬Ņ²æÉÓĆĶØČė×ćĮæµÄijĘųĢåµÄ·½·ØĄ““śĢę”£ĶØČėĘųĢåŹ±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ .
£Ø4£©ÅØĖõĖłµĆµÄNaOHČÜŅŗÓÉÓŚĪüŹÕĮĖæÕĘųÖŠµÄCO2¶ųŗ¬ÓŠŌÓÖŹ£¬øĆŌÓÖŹæÉĶعżæĮ»Æ·“Ó¦³żČ„£¬Š“³öæĮ»Æ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø5£©øĆÉś²śĮ÷³ĢÄÜŹµĻÖ £ØĢī»ÆѧŹ½£©µÄŃ»·ĄūÓĆ”£
£Ø6£©Ńõ»ÆĀĮŹĒ¹¤ŅµÉĻŅ±Į¶ĀĮµÄŌĮĻ£¬ÓĆŃõ»ÆĀĮµē½āÖʱø½šŹōĀĮŹ±Šč¼ÓČė±ł¾§ŹÆ£ØNa3AlF6£©×÷ÖśČŪ¼Į£¬Š“³öÓĆNaFŗĶAl2(SO4)3·“Ó¦Öʱø±ł¾§ŹÆµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½ĖÕŹ”Ģ©ÖŻŹŠ½ŖŃßĒųø߶žÉĻŃ§ĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£ØŃ”ŠŽ£©£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©Õė¶Ō»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ½ā¾öĻĀĮŠĪŹĢā”£
£Ø1£©²ā¶ØĻ”ĮņĖįŗĶĻ”ĒāŃõ»ÆÄĘÖŠŗĶČČ£ØÖŠŗĶČČĪŖ57.3 kJ”¤mol£1£©µÄŹµŃé×°ÖĆČēĶ¼ĖłŹ¾”£
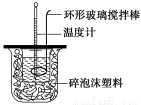
ijŠĖȤŠ”×éµÄŹµŃ鏿ֵ½į¹ūŠ”ÓŚ57.3 kJ”¤mol£1£¬ŌŅņæÉÄÜŹĒ (Ģī×ÖÄø)”£
a£®ŹµŃé×°ÖƱ£ĪĀ”¢øōČČŠ§¹ū²ī
b£®¶ĮČ”»ģŗĻŅŗµÄ×īøßĪĀ¶Č¼ĒĪŖÖÕµćĪĀ¶Č
c£®·Ö¶ą“Ī°ŃNaOHČÜŅŗµ¹ČėŹ¢ÓŠĮņĖįµÄŠ”ÉÕ±ÖŠ
d£®ÓĆĪĀ¶Č¼Ę²ā¶ØNaOHČÜŅŗĘšŹ¼ĪĀ¶ČŗóĪ“Ļ“µÓ£¬Ö±½Ó²ā¶Ø
H2SO4ČÜŅŗµÄĪĀ¶Č
£Ø2£©ĄūÓĆĒāĘųæÉŅŌÖĘČ”¹¤ŅµŌĮĻŅŅĖį”£ŅŃÖŖ£ŗ
a£®CH3COOH(l)+2O2(g) ==2CO2(g)+2H2O(l) ”÷H = ”Ŗ870.3kJ/mo1
b£®C(s)+O2(g) ==CO2(g) ”÷H = ”Ŗ393.5kJ/mo1
c£®H2(g) +1/2 O2(g)==H2O(l) ”÷H = ”Ŗ285.8kJ/mo1
¢ŁĻąĶ¬ÖŹĮæµÄCH3COOH”¢C”¢H2ĶźČ«Č¼ÉÕŹ±£¬·Å³öČČĮæ×ī¶ąµÄŹĒ ”£
¢ŚĄūÓĆÉĻŹöŠÅĻ¢¼ĘĖćĻĀŹö·“Ó¦£ŗ2C(s)+2H2(g)+O2(g)=CH3COOH(l) ”÷H= kJ/mol”£
£Ø3£©ÓĆCl2Éś²śÄ³Š©ŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśø±²śĪļHCl”£ĄūÓĆ·“Ó¦A£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
·“Ó¦A£ŗ4HCl£«O2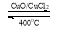 2Cl2£«2H2O
2Cl2£«2H2O
ŅŃÖŖ£ŗ¢”£®“ĖĢõ¼žĻĀ·“Ó¦AÖŠ£¬4 mol HCl±»Ńõ»Æ£¬·Å³ö115.6 kJµÄČČĮ攣
¢¢£®
¢ŁŠ“³ö“ĖĢõ¼žĻĀ£¬·“Ó¦AµÄČČ»Æѧ·½³ĢŹ½__________________ _______”£
¢Ś¶ĻæŖ1 mol H”ŖO¼üÓė¶ĻæŖ1 mol H”ŖCl¼üĖłŠčÄÜĮæĻą²īŌ¼ĪŖ kJ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com