
下列关于有机物的说法正确的是( )
A. 聚丙烯能使酸性高锰酸钾溶液褪色
B. 分馏石油得到的各馏分都是纯净物
C. 蛋白质水解和油脂皂化都是高分子转化成小分子的过程
D. C4H10有2种同分异构体
科目:高中化学 来源:2015-2016学年辽宁省大连市高二下期末化学试卷(解析版) 题型:选择题
选项 | 实验操作 | 现象 | 结论 |
A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32﹣ |
B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸 一定没有发生化学反应 |
C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 不能说明该食盐中一定没有添加碘化钾 |
D | 向盛有25mL沸水的烧杯中滴加5﹣6滴FeCl3饱和溶液,继续煮沸 | 溶液生成红褐色沉淀 | 制得Fe(OH)3胶体 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源:2017届湖南长沙一中高二上第一次月考(开学考试)化学卷(解析版) 题型:实验题
回归、改进、拓展教材实验,是高考化学实验考查的常见形式。
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。
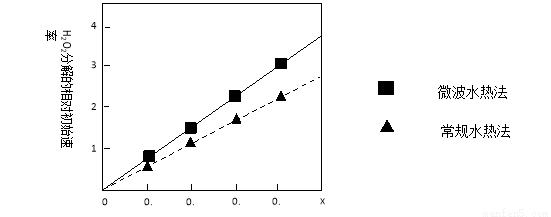
II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):
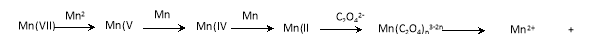
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s)[K] | |||
0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下学期期末化学卷(解析版) 题型:填空题
在电解冶炼铝的过程中加入冰晶石,可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3===2Na3AlF6+3CO2↑+9H2O。根据题意完成下列填空:
(1) (3分)冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在________(填序号)。
a.离子键 b.极性键 c.配位键 d.范德华力
(2) (3分)CO2分子的空间构型为____________,中心原子的杂化方式为____________,和CO2 互为等电子体的氧化物是________。
(3) (2分)反应物中电负性最大的元素为_______(填元素符号),写出其原子最外层的电子排布图:____________。
(4) (2分)冰晶石由两种微粒构成,冰晶石的晶胞结构如图Z164甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是________(填具体的微粒符号)。


图Z164
(5) (5分)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
若已知Al的原子半径为d,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为________个;Al晶体的密度为______________________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下学期期末化学卷(解析版) 题型:选择题
下列几组顺序排列不正确的是( )
A. 沸点高低:HI>HBr>HCl>HF
B. 热稳定性大小:HF>H2O>NH3>PH3
C. 熔点高低:金刚石>食盐>金属钠>冰
D. 微粒半径大小:S2->Cl->F->Na+>Al3+
查看答案和解析>>
科目:高中化学 来源:2016届甘肃天水一中学高二下期末(高三开学)考化学(解析版) 题型:实验题
(1)计算结果:需要称取NaOH固体 g;
(2)配制时,必须使用的上述仪器有 (填代号);
(3)配制时,其正确的操作顺序是(数字序号表示,每个操作只用一次) ;
① 用少量水洗涤烧杯2 ~ 3次,洗涤液均注入容量瓶,振荡
② 在盛有NaOH固体的烧杯中加入适量水溶解
③ 将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
④ 将容量瓶盖紧,反复上下颠倒,摇匀
⑤ 改用胶头滴管加水,使溶液凹面恰好与刻度相切
⑥ 继续往容量瓶内小心加水,直到液面接近刻度1 ~ 2cm处
(4)若出现如下情况,其中将引起所配溶液浓度偏高的是 (填下列编号)。
①容量瓶实验前用蒸馏水洗干净,但未烘干 ②定容观察液面时俯视
③溶解过程中物质放热,没有等至室温配置 ④加蒸馏水时不慎超过了刻度
(5)容量瓶不能用于__________(填下列序号)。
① 配制一定体积准确浓度的标准溶液
② 贮存溶液
③ 测量容量瓶规格以下的任意体积的液体
④ 准确稀释某一浓度的溶液
⑤ 用来加热溶解固体溶质
II.(共6分)某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
(1)甲和乙两位同学分别设计了如下图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用______(填“甲”或“乙”)装置。理由是 。
(2)实验中浓硫酸的作用是________________。
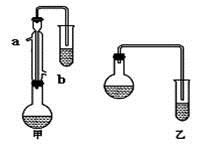
(3)反应物CH3OH应过量,理由是 。
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称。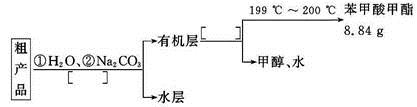
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫市海原一中高一下第二次月考化学试卷(解析版) 题型:填空题
某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
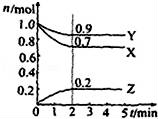
(1)该反应的化学方程式为: ;
(2)反应开始至2min,用Z表示的平均反应速率为: ;
(3)下列叙述能说明上述反应达到化学平衡状态的是 (填序号).
A.各物质的浓度不随时间的变化而变化
B.单位时间内每消耗3mol X,同时生成3mol X
C.X,Y,Z的浓度之比为1:1:1
D.反应已经停止
(4)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g)+Y(g)═2Z(g),当改变下列条件时,反应速率会发生什么变化?(选填“增大”、“减小”或“不变”)
①在其它条件不变时 降低温度: ;
②在其它条件不变时加入催化剂: .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏勤行校区高二下第二次月考化学试卷(解析版) 题型:选择题
二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
A. 利用金属钠或者金属钾
B. 利用质谱法
C. 利用红外光谱法
D. 利用核磁共振氢谱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com