
| A.1.0 mol | B.1.6 mol | C.2.2 mol | D.2.4 mol |
科目:高中化学 来源:不详 题型:单选题
| A.0.15 mol·L-1 | B.0.225 mol·L-1 |
| C.0.3 mol·L-1 | D.0.6 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
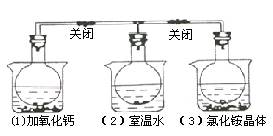
A.2NO2 N2O4是放热反应 N2O4是放热反应 | B.NH4Cl溶于水时放出热量 |
| C.烧瓶(1)中平衡混合气的相对分子质量增大 | D.烧瓶(3)中气体的压强增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题



| A.amol | B.(0.1+a)mol | C.(0.05+a)mol | D.(0.2+a)mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuNH4SO3 | B.Cu(NH4)2(SO4)2 | C.Cu3(NH4)2(SO4)3 | D.Cu(NH4)2(S2O3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO是红棕色气体 | B.常温下氮气与氧气反应可生成NO |
| C.NO溶于水可以生成硝酸 | D.NO是汽车尾气的有害成分之一 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com