
 .
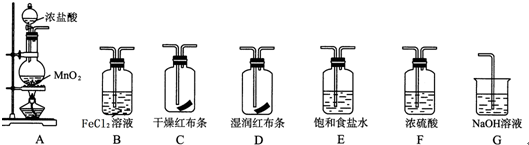
. 分析 (1)实验室用A装置制备氯气,经过除杂E装置、干燥F装置后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气;
(2)饱和食盐水能抑制氯气的溶解,吸收氯化氢;氯气有毒,需要进行尾气处理,氯气能够与碱反应,可以用碱吸收过量氯气;次氯酸具有漂白性;
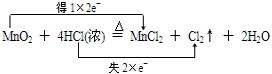
(3)氯气具有强的氧化性,能够与氯化亚铁反应生成氯化铁;氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
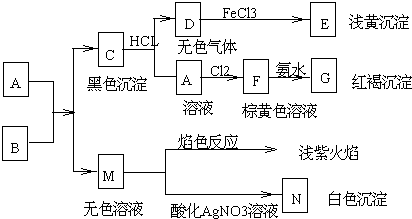
(4)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,反应中二氧化锰中+4 价锰元素化合价降为氯化锰中+2价,降2价,4mol氯化氢参加反应,只有2mol氯化氢中-1价氯元素化合价升高为氯气 中的0价,据此用双线桥表示.
解答 解:(1)实验室用A装置制备氯气,经过除杂E装置、干燥F装置后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气,则各仪器从左至右的连接顺序为A、E、F、C、D、B、G,
故答案为:A E F C D B G;
(2)浓盐酸有挥发性,所以氯气中含有氯化氢气体,因饱和食盐水中含有大量的Cl-,对Cl2的溶解有抑制作用,使Cl2+H2O?H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;
氯气有毒,需要进行尾气处理,氯气能够与碱反应,可以用氢氧化钠溶液吸收过量氯气,防止污染环境;
氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;
故答案为:吸收Cl2中的HCl气体; 吸收尾气Cl2,防止污染环境;红色褪去;
(3)氯气具有强的氧化性,能够与氯化亚铁反应生成氯化铁,离子方程式:2Fe2++Cl2═2Fe3++2Cl-;氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O;
故答案为:2Fe2++Cl2═2Fe3++2Cl- Cl2+2OH-═Cl-+ClO-+H2O;
(4)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,反应中二氧化锰中+4 价锰元素化合价降为氯化锰中+2价,降2价,4mol氯化氢参加反应,只有2mol氯化氢中-1价氯元素化合价升高为氯气 中的0价,用双线桥表示为: ;
;
故答案为: .
.
点评 本题考查氯气的制备、性质的检验,明确氯气制备原理及氯气、次氯酸的化学性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸甲酯的结构简式:CH2O | |
| B. | Na+的.结构示意图: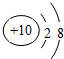 | |
| C. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | CO2的电子式为: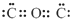 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF | |
| B. | 若将0.2 mol•L-1Na2CO3和0.1 mol•L-1NaHCO3溶液等体积混合,则溶液中:3c(OHˉ)=3c(H+)+2c(HCO3ˉ)+5c(H2CO3)+c(CO32ˉ) | |
| C. | 根据上表,反应ClOˉ+H2O?HClO+OHˉ的水解常数Kh≈10ˉ7.6 | |
| D. | 向上述NaClO 溶液中通HF气体至恰好完全反应时:c(Na+)>c(Fˉ)>c(H+)>c(HClO)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
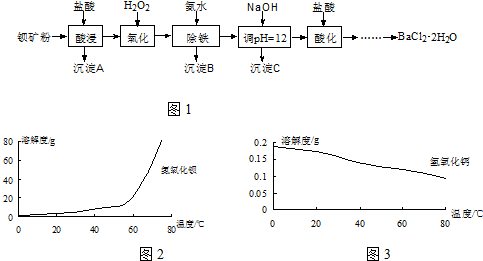
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
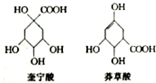 奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )
奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )| A. | 奎宁酸的相对分子质量比莽草酸的大18 | |
| B. | 可用高锰酸钾溶液鉴别奎宁酸和莽草酸 | |
| C. | 等物质的量的奎宁酸和莽草酸分别与足量Na反应,同温同压下产生H2的体积比为4:5 | |
| D. | 等物质的量的两种分别与足量NaOH溶液反应,消耗NaOH的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
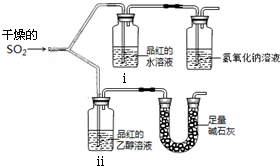 实验小组为探究SO2的漂白性和还原性,设计了以下实验.完成下列填空:
实验小组为探究SO2的漂白性和还原性,设计了以下实验.完成下列填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com