
| A. | 碳酸钠与次氯酸反应:CO32-+2HClO═2ClO-+H2O+CO2↑ | |
| B. | 二氧化硫通入次氯酸钠溶液中:SO2+ClO-+2OH-═SO42-+Cl-+H2O | |
| C. | 明矾溶液中加氢氧化钡溶液至硫酸根恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O | |
| D. | 碘化亚铁溶液与少量氯气反应:2I-+Cl2=I2+2Cl- |
分析 A.不符合反应客观事实.
B.二氧化硫具有还原性,能够被次氯酸根离子氧化生成硫酸根离子;
C.明矾溶液中加氢氧化钡溶液至硫酸根恰好沉淀完全,反应生成偏铝酸价、硫酸钡和水;
D.碘离子还原性强于二价铁离子,氯气少量先氧化碘离子.
解答 解:A.次氯酸酸性强于碳酸氢钠弱于碳酸,依据强酸制备弱酸规律,Na2CO3溶液中加入HClO溶液:CO32-+HClO═HCO3-+ClO-,故A错误;
B.足量的二氧化硫与次氯酸钠反应方程式为:SO2+ClO-+2OH-═SO42-+Cl-+H2O,故B正确;
C.明矾溶液中加氢氧化钡溶液至硫酸根恰好沉淀完全,离子方程式:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O,故C正确;
D.碘化亚铁溶液与少量氯气反应,离子方程式:2I-+Cl2=I2+2Cl-,故D正确;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,注意离子反应遵循客观事实,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaAlO2溶液中通入过量CO2气体:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| B. | NH4 HCO3溶液与足量的NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 向FeI2溶液中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 6 | C. | 8 | D. | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 常压下五种元素的单质中Z单质的沸点最高 | |
| B. | X的氢化物的沸点比W的氢化物的沸点低 | |
| C. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| D. | X、Y元素的氢化物都能与该元素的最高价氧化物的水化物浓溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用葡萄糖制镜或保温瓶胆 | B. | 用Na2S除去废水中的Hg2+ | ||
| C. | 用Na2SiO3溶液制备木材防火剂 | D. | 用K2FeO4作为高效水处理剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液:NH4+,Ca2+,NO3-,Cl- | |
| B. | c(OH-)=1×10-13mol•L-1的溶液:Na+,K-,ClO-,SO42- | |
| C. | 0.1mol•L-1的FeCl2溶液:K+,Na+,SO42-,Br- | |
| D. | 0.1mol•L-1的酸性KMnO4溶液:Na+,Mg2+,NO3-,SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有10个中子的氧原子:818O | |
| B. | HF的电子式:H+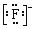 | |
| C. | Cl-离子的结构示意图: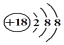 | |
| D. | N2的结构式::N≡N: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ④③①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com