
下列各组离子中,在酸性溶液中能大量共存,且溶液为无色透明的是
A.K+、MnO4-、Cl-、SO42- B.Na+、CO32-、 Cl-、SO42-
C.NO3-、Na+、HCO3-、Ba2+ D.Na+、NO3-、NH4+、SO42-
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学文科试卷(解析版) 题型:选择题
红葡萄酒密封时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。下列能与乙醇反应生成酯的物质是
A.苯 B.乙烯 C.乙酸 D.甲烷
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学理科试卷(解析版) 题型:选择题
下列叙述中,能证明某物质是弱电解质的是
A.熔化时不导电
B.不是离子化合物,而是极性共价化合物
C.水溶液的导电能力很差
D.溶液中已电离的离子和未电离的分子共存
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:选择题
下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是
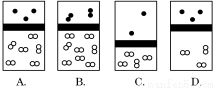
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的有( )个
⑴澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
⑵氢氧化钡与硫酸反应:OH-+H+=H2O
⑶铜片与硝酸银溶液反应:Cu+Ag+=Cu2++Ag
⑷氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-=Mg(OH)2↓
⑸铁片投入稀盐酸中:2Fe+6H+=2Fe3++3H2↑
⑹氨水与盐酸的反应:OH-+H+=H2O
⑺碳酸氢钠与盐酸反应:HCO3-+H+=CO2↑+H2O
⑻Na2O与水反应:O2-+H2O=2OH-
⑼少量的NH4HSO4溶液与Ba(OH)2溶液的反应:NH4++H++SO42-+Ba2++2OH-=NH3.H2O+H2O+BaSO4↓
⑽向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性: 2H++SO42-+Ba2++2OH-= 2H2O+BaSO4↓
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:填空题
(8分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl- ,
(2)由第二份进行的实验可知混合物中应含 离子,其物质的量浓度为 。
(3)由第三份进行的实验可知12.54g 沉淀的成份为 。请计算形成该沉淀的原混合物中各离子的物质的量 。
(4)综合上述实验,你认为以下结论正确的是( )
A.该混合物中一定含有K+、NH4+、CO32-、SO42-,可能含有Cl-,且n(K+)≥0.04mol
B.该混合物中一定含有NH4+、CO32-、SO42-,可能含有Ca2+、 K+、Cl-
C.该混合物中一定含有NH4+、CO32-、SO42-,可能含有K+、Cl-
D.该混合物中一定含有NH4+、SO42-,可能含有Ca2+、K+、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:选择题
关于O2与O3气体,下列比值一定为2:3的是
A.若两种气体所占体积相同,两种气体的质量之比
B.若温度和压强相同,两种气体的密度之比
C.若两种两种气体原子数相同,两种气体的质子数之比
D.若两种气体的质量相同,两种气体的分子数之比
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:选择题
我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫“铝铍测年法”。下列有关26Al和10Be的说法正确的是
A.10Be和9Be是中子数不同质子数相同的同种核素
B.10Be的原子核内质子数等于中子数
C.5.2 g 26Al3+中所含的电子数约为1.2×1024
D.26Al和26Mg的质子数和核外电子数均不同,中子数相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省岳阳市高三教学质量检测化学试卷(解析版) 题型:填空题
(10分)铜及其化合物在工农业生产及日常生活中应用非常广泛。
(1)由辉铜矿制取铜的反应过程为:
2Cu2S(s) + 3O2 (g) = 2Cu2O(s) + 2SO2(g) △H = -768.2kJ·mol-1,
2Cu2O(s) + Cu2S(s) = 6Cu(s) + SO2(g) △H = +116.0kJ·mol-1,
请写出Cu2S与O2反应生成Cu与SO2的热反应方程式: 。
(2)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图。

①当c(Cl-)=9 mol·L-1时,溶液中主要的3种含铜物种浓度大小关系为 。
②在c(Cl-)=1 mol·L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为 (任写一个)。
(3) 电解Na2HPO3溶液可得到亚磷酸,装置如下图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过)

①阳极的电极反应式为: ____________。
②产品室中反应的离子方程式为: _____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com