
�������������й㷺��Ӧ�ã�ij����������Ϊ��Ҫԭ���������ᡣ
��֪����550��ʱ��![]()
![]()
��һ���¶��£��������ڿ��������տ��ܷ������з�Ӧ(�������![]() ��
��![]() �����
�����
��Ϊ4��1)��![]() ,
,![]()
(1) 550��ʱ��6��4 g ![]() ������
������![]() ��ַ�Ӧ����
��ַ�Ӧ����![]() ���ų�����
���ų�����
9��83 kJ
(����ڡ��������ڡ���С�ڡ�)o
(2)��ʹ��Ӧ�ٵ�ƽ��������Ӧ�����ƶ������д�ʩ���е��� ��(����ĸ)
a����ƽ�������г���![]() b����ƽ�������г���
b����ƽ�������г���![]()
c���ı䷴Ӧ�Ĵ��� d�����ͷ�Ӧ���¶�
(3)Ϊʹ![]() ��ȫ����
��ȫ����![]() ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����
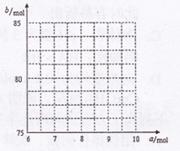 ��������������50��ʱ������¯����
��������������50��ʱ������¯����![]() ��
��
��������Ƕ���?
(4)720 g������![]() �ڿ�������ȫ���գ����ù���
�ڿ�������ȫ���գ����ù���
��![]() ��
��![]() �����ʵ���֮��n(
�����ʵ���֮��n(![]() )��n(
)��n(![]() )=6:
)=6: ![]() ��
��
��ʱ���Ŀ���Ϊ![]() mol��
mol��
����д������ڵĹ�ϵʽ�� ��
��������ͼ�л���![]() ��
��![]() �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�꽭��ʡ�����и��������ε��п��ԣ���ѧ���⣩ ���ͣ������
�������������й㷺��Ӧ�ã�ij����������Ϊ��Ҫԭ���������ᡣ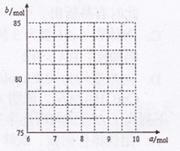
��֪����550��ʱ��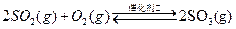
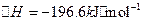
��һ���¶��£��������ڿ��������տ��ܷ������з�Ӧ(�������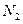 ��
��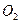 �����
�����
��Ϊ4��1)��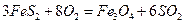 ,
,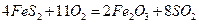
(1) 550��ʱ��6��4 g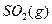 ������
������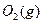 ��ַ�Ӧ����
��ַ�Ӧ����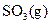 ���ų�����
���ų�����
9��83 kJ
(����ڡ��������ڡ���С�ڡ�)o
(2)��ʹ��Ӧ�ٵ�ƽ��������Ӧ�����ƶ������д�ʩ���е��� ��(����ĸ)
a����ƽ�������г���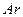 b����ƽ�������г���
b����ƽ�������г���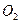
c���ı䷴Ӧ�Ĵ��� d�����ͷ�Ӧ���¶�
(3)Ϊʹ ��ȫ����
��ȫ����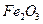 ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����
��������������50��ʱ������¯����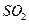 ��
��
��������Ƕ���?
(4)720 g������ �ڿ�������ȫ���գ����ù���
�ڿ�������ȫ���գ����ù���
��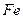 ��
��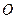 �����ʵ���֮��n(
�����ʵ���֮��n(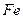 )��n(
)��n(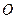 )="6:"
)="6:"  ��
��
��ʱ���Ŀ���Ϊ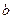 mol��
mol��
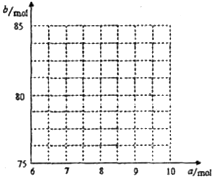
����д������ڵĹ�ϵʽ�� ��
��������ͼ�л���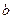 ��
�� �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������й㷺��Ӧ�ã�ij����������Ϊ��Ҫԭ���������ᡣ
��֪����550��ʱ��![]() ��H=-196.6KJ��mol-1
��H=-196.6KJ��mol-1
��һ���¶��£��������ڿ��������տ��ܷ������з�Ӧ(�������N2��O2�����
��Ϊ4��1)��![]() ,
,![]()
(1) 550��ʱ��6��4 g SO2(g)������O2(g)��ַ�Ӧ����SO3(g)���ų�����
9��83 kJ (����ڡ��������ڡ���С�ڡ�)��
(2)��ʹ��Ӧ�ٵ�ƽ��������Ӧ�����ƶ������д�ʩ���е��� ��(����ĸ)
a����ƽ�������г���Ar b����ƽ�������г���O2
c���ı䷴Ӧ�Ĵ��� d�����ͷ�Ӧ���¶�
(3)ΪʹFeS2��ȫ����Fe2O3������ʱҪʹ�ù����Ŀ�������������50��ʱ������¯����SO2����������Ƕ���?
(4)720 g������FeS2�ڿ�������ȫ���գ����ù�����Fe��O�����ʵ���֮��n(Fe)��n(O)=6: ![]() ��
��
��ʱ���Ŀ���Ϊ![]() mol��
mol��
����д��a��b�Ĺ�ϵʽ�� ��
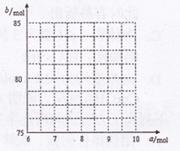
��������ͼ�л���![]() ��
��![]() �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(10��)�������������й㷺��Ӧ�ã�ij����������Ϊ��Ҫԭ���������ᡣ
��֪����550��ʱ��![]()
![]()
��һ���¶��£��������ڿ��������տ��ܷ������з�Ӧ(�������![]() ��
��![]() �����
�����
��Ϊ4��1)��![]() ,
,![]()
(1) 550��ʱ��6��4 g ![]() ������
������![]() ��ַ�Ӧ����
��ַ�Ӧ����![]() ���ų�����
���ų�����
9��83 kJ
(����ڡ��������ڡ���С�ڡ�)o
(2)��ʹ��Ӧ�ٵ�ƽ��������Ӧ�����ƶ������д�ʩ���е��� ��(����ĸ)
a����ƽ�������г���![]() b����ƽ�������г���
b����ƽ�������г���![]()
c���ı䷴Ӧ�Ĵ��� d�����ͷ�Ӧ���¶�
(3)Ϊʹ![]() ��ȫ����
��ȫ����![]() ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����
 ��������������50��ʱ������¯����
��������������50��ʱ������¯����![]() ��
��
��������Ƕ���?
(4)720 g������![]() �ڿ�������ȫ���գ����ù���
�ڿ�������ȫ���գ����ù���
��![]() ��
��![]() �����ʵ���֮��n(
�����ʵ���֮��n(![]() )��n(
)��n(![]() )=6:
)=6: ![]() ��
��
��ʱ���Ŀ���Ϊ![]() mol��
mol��
����д������ڵĹ�ϵʽ�� ��
��������ͼ�л���![]() ��
��![]() �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com