
【题目】Ⅰ.(1)如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134KJ/mol,E2=368KJ/mol( E1、 E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 、 (填“增大”、“减小”或“不变”)。写出该 反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可
Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
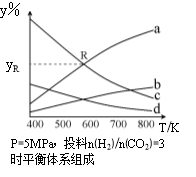
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大
B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变
D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2 C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
【答案】I 减小 不变 NO2(g)+CO(g)=NO(g)+CO2(g)△H=—234kJ/mol
Ⅱ (1)b (2)B C (3) A C (4 37.5% (或0.375或3/8)
【解析】I(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368kJ-134kJ=234kJ,反应热化学方程式为△H=—234kJ/mol;
(2)反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)是熵减的反应即△S<0,若150℃下能自发进行根据△G=△H-T△S<0可知△H一定小于0;
Ⅱ.(1)乙醇是生成物,氢气也是生成物,但氢气的浓度是乙醇的3倍,则表示CH3CH2OH体积分数曲线的是b。
(2)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A.平衡常数K只与温度有关系,A错误;B.CO2的转化率不再增大,说明正逆反应速率相等,达到平衡状态,B正确;C. 混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,因此当混合气体的平均相对分子质量不再改变时可以说明反应达到平衡状态,C正确;D.可逆反应中反应物不可能完全转化为生成物,D错误,答案选BC。
(3)根据方程式可知正方应是体积减小的、吸热的可逆反应,则其他条件恒定,达到平衡后,能提高H2转化率的措施是升高温度或移去乙醇,充入更多的H2平衡向正反应方向移动,但氢气的转化率降低,增大容器体积,压强降低,平衡向逆反应方向进行,转化率降低,答案选AC。
(4)根据图像可知图中曲线a和c的交点R表示氢气和水蒸气的含量相等,则
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g)
CH3CH2OH(g)+3H2O(g)
起始量(mol) 1 3 0 0
转化量(mol) x 3x 0.5x 1.5x
平衡量(mol)1—x 3—3x 0.5x 1.5x
则有3—3x=1.5x
解得x=2/3
则yR=![]() 。
。


科目:高中化学 来源: 题型:
【题目】(1)工业上用FeCl3溶液刻蚀铜的线路板,反应为Cu+2FeCl3= CuCl2+ 2FeCl2 依据此氧化还原反应,设计成原电池。现给出铁棒、铜棒、石墨电极,原电池的负极为 ,正极电极反应方程式 ,若负极减重6.4克,则电路中转移电子的物质的量为 。
(2)在一密闭的2L的容器里装有4mol SO2和2mol O2,在一定条件下开始反应。2min末测得容器中共有5.6mol 气体,试计算:
(1)2min末SO3的浓度 。
(2)用SO2表示该反应的平均反应速率 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法符合事实的是
A.物质的量浓度相同的硫酸氢铵溶液和醋酸铵溶液中,硫酸氢铵中的铵根离子物质的量浓度较小
B.在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
C.物质的量浓度均为0.02 mol/L的弱酸HX及其盐NaX等体积混合后:c(X-)+ c(HX)= 0.02 mol/L
D.己知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12。在含C1-、CrO42-浓度相同的溶液中滴加AgNO3溶液时,首先生成Ag2CrO4沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)键线式![]() 表示的分子式是 ;名称是 。
表示的分子式是 ;名称是 。
(2) 中含有的官能团的名称为 。
中含有的官能团的名称为 。
(3)化学式为C3H8O的醇在一定条件下能氧化成醛,写出此反应的化学方程式_________ __
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A+B![]() mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:

(1)温度T1________T2(填“大于”“等于”或“小于”)。
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2(填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强________(填“增大”“减小”或“不变”),平衡___ _____移动(填“向正反应方向”“向逆反应方向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列几组物质,请将其字母按要求填入空格内:
A.CH2=CH—COOH和油酸(C17H33COOH)
B.乙醇和乙二醇
C.淀粉和纤维素
D.![]()
E.
F.![]()
① 互为同系物的是 。
② 互为同分异构体的是 。
③ 既不是同系物,也不是同分异构体,但可看成是同一类物质的是 。
(2)现有下列物质,请将其字母按要求填入空格内:
A.淀粉 B.葡萄糖 C.蛋白质 D.油脂
① 遇I2变蓝的是 。
② 遇浓HNO3呈黄色的是 。
③ 能发生皂化反应制取肥皂的是 。
④ 加热条件下能与新制的氢氧化铜反应生成红色沉淀的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选修一物质结构与性质过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉做显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:4FeCl3+2NH2OHHCl═4FeCl2+N2O↑+6HCl+H2O
①基态Fe原子中,电子占有的最高能层符号为____________,核外未成对电子数为____________ ,Fe3+在基态时,外围电子排布图为____________。
②羟胺中(NH2OH)采用sp3杂化的原子有____________,三种元素电负性由大到小的顺序为____________;与ClO4-互为等电子体的分子的化学式为____________。
(2)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合18电子规则.如Cr可以与CO形成Cr(CO)6分子:价电子总数(18)=Cr的价电子数(6)+CO提供电子数(2×6)。
Fe、Ni两种原子都能与CO形成配合物,其化学式分别为____________、____________。
(3)Pt2+的常见配合物Pt(NH3)2Cl2存在两种不同的结构:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度较小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是____________分子(选填“极性”或“非极性”)。
②P分子的结构简式为____________。
(4)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为a pm.晶胞中两个Ni原子之间的最短距离为____________ pm。若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式_______________________。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为___________(填化学式);
②NaH2PO2为___________(填“正盐”或“酸式盐”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________。
(4)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式_________________ ___________________;
②分析产品室可得到H3PO2的原因__________________ _________________;
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有 杂质,该杂质产生的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H12O的饱和一元醇分子中有两个“CH3”、一个“CH”、两个“CH2”和一个“OH”,可能的结构有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com