
某溶液中除了H+、OH﹣以外,还含有大量的Mg2+、Fe3+、Cl﹣,且这三种离子的物质的量浓度之比为1:1:6,下列有关该溶液判断正确的是( )
A. 向该溶液中加入KI溶液后,原有的5种离子的物质的量不变
B. 向该溶液中滴加稀NaOH溶液,立即出现白色沉淀
C. 向该溶液中加入过量铁粉,只发生置换反应
D. 若溶液中c (Cl﹣)=0.6mol/L,则该溶液的pH=1
考点: 常见离子的检验方法.
专题: 物质的量浓度和溶解度专题.
分析: 某溶液中除H+、OH﹣外,还含有大量的Mg2+、Fe3+、Cl﹣,且这三种离子的物质的量浓度之比为1:1:6,由Mg2+、Fe3+、Cl﹣所带的电荷2×1+3×1<1×6可知,溶液为酸性溶液,是氯化镁、氯化铁、氯化氢的混合溶液.
A、Fe3+有强氧化性,能氧化I﹣为I2.
B、溶液呈酸性,氢氧化钠先中和盐酸.
C、铁除置换氢气外,Fe3+有强氧化性,能与Fe反应生成Fe2+;
D、根据电荷守恒计算氯化氢产生的氢离子浓度,在根据PH=﹣logc(H+)计算.
解答: 解:某溶液中除H+、OH﹣外,还含有大量的Mg2+、Fe3+、Cl﹣,且这三种离子的物质的量浓度之比为1:1:6,由Mg2+、Fe3+、Cl﹣所带的电荷2×1+3×1<1×6可知,溶液为酸性溶液,是氯化镁、氯化铁、氯化氢的混合溶液.
A、Fe3+有强氧化性,能氧化I﹣为I2,溶液中加入KI溶液后,Fe3+离子物质的量发生变化,故A错误;
B、溶液为酸性溶液,是氯化镁、氯化铁、氯化氢的混合溶液,氢氧化钠先中和盐酸,再发生沉淀反应,故B错误;
C、溶液中Fe3+有强氧化性,铁除置换氢气外,还能与Fe3+反应生成Fe2+,故C错误.
D、若溶液中c(Cl﹣)=0.6 mol/L,则c(Mg2+)=0.1mol/L,c(Fe3+)=0.1mol/L,则c(H+)×1+c(Mg2+)×2+c(Fe3+)×3=c(Cl﹣)×1,即c(H+)×1+0.1mol/L×2+0.1mol/L×3=0.6mol/L×1,解得c(H+)=0.1mol/L,所以溶液pH=﹣logc(H+)=1,故D正确;
故选D.
点评: 本题考查溶液中离子共存问题、溶液计算等,难度中等,判断溶液是氯化镁、氯化铁、氯化氢的混合溶液是解题关键.


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
1mol某有机物充分燃烧,只生成88g二氧化碳气体和54g水,下列正确的是( )
A. 该有机物的分子式为CH4
B. 该有机物的分子式一定为C2H6
C. 该有机物的分子式一定为C2H6O
D. 该有机物的分子中碳原子和氢原子的个数比为1:3,可能含有氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Mg2+、Ba2+、CO32﹣、SO42﹣、Cl﹣,现取三份100mL溶液进行如下实验:根据上述实验,以下推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
第二份加足量KOH溶液加热后,收集到气体0.08mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
A. Na+一定存在
B. 100mL溶液中含0.01mol CO32﹣
C. Cl﹣一定存在
D. Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有的离子可能是K+、Ba2+、A13+、Mg2+、AlO2﹣、CO32﹣、SiO32﹣、Cl﹣中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成.
②另取少量原溶液,逐滴加入5mL0.2mol•L﹣1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失.
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43g.
下列说法中正确的是( )
A. 该溶液中一定不含Ba2+、Mg2+、A13+、SiO32﹣、Cl﹣
B. 该溶液中一定含有K+、AlO2﹣、CO32﹣、Cl﹣
C. 该溶液是否有K+需做焰色反应(透过蓝色钴玻璃片)
D. 可能含有Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
含有Ag+、Al3+、Mg2+、Ba2+等四种金属离子的混合溶液.欲使上述四种离子分别以沉淀形式从溶液中分离出来.下列加入试剂的顺序能达到实验目的是( )
A. NaOH、NaCl、HCl、Na2SO4 B. NaCl、Na2SO4、NaOH、HCl
C. NaCl、NaOH、Na2SO4、HCl D. Na2SO4、NaOH、NaCl、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、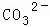 、
、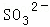 、
、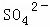 、Cl﹣、
、Cl﹣、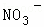 中的一种或几种,取该溶液进行迂续实验,实验内容如下:
中的一种或几种,取该溶液进行迂续实验,实验内容如下:
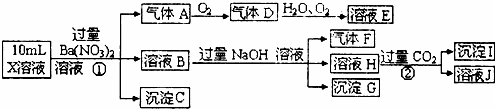
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是 ,不能确定是否含有的离子是,若要确定其中阳离子的存在,最可靠的化学方法是 .
沉淀G的化学式为.
(3)写出有关离子方程式:
步骤①中生成A.
步骤②生成沉淀I.
(4)假设测定A、F、I均为0.01mol,10mLX溶液中n(H+)=0.04mol,而沉淀C物质的量0.07mol,能说明(1)中不能确定的阴离子存在的理由是. .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,下列叙述正确的是()
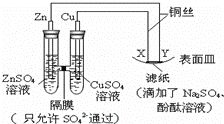
A. Y为阴极,发生还原反应 B. X为正极,发生氧化反应
C. Y与滤纸接触处有氧气生成 D. X与滤纸接触处变红
查看答案和解析>>
科目:高中化学 来源: 题型:
I.按系统命名法填写下列有机物的名称或结构简式:
(1)CH3CH(C2H5)CH(CH3)CH2 CH(CH2CH3)2 ;
(2)2﹣甲基﹣4﹣乙基﹣3﹣己烯 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com