
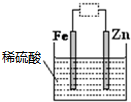
| A、虚线框中接直流电源,铁可能会被腐蚀 |
| B、虚线框中接灵敏电流计或接直流电源,锌都是负极 |
| C、虚线框中接灵敏电流计,该装置可将化学能转化为电能 |
| D、若将电解液改成硫酸锌溶液并接上直流电源,该装置可用于铁皮上镀锌 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、最外层有2个电子的原子都是金属原子 |
| B、非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数 |
| C、非金属元素呈现的最高化合价不超过该元素原子的最外层电子数 |
| D、最外层有5个电子的原子都是非金属原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、石灰水与过量碳酸氢钠溶液反应:HCO
| ||||
B、向沸水中滴加饱和的FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O
| ||||
| C、氧化铜与稀硫酸反应:2H++O2-═H2O | ||||
D、碳酸氢钠溶液中加入盐酸:CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ν正(A)=3 ν逆(B) |
| B、单位时间内生成n molA,同时生成3n molB |
| C、容器内混合气体的平均相对分子质量不变 |
| D、容器内混合气体的密度不随时间而改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不能用植物油萃取溴水中的溴 |
| B、皂化是高分子生成小分子的过程 |
| C、和H2加成后能提高其熔点及稳定性 |
| D、水解可得到丙三醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
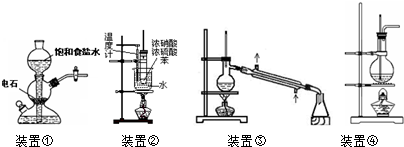
| A、装置①:实验室中若需制备较多量的乙炔可用此装置 |
| B、装置②:实验室中可用此装置来制备硝基苯,但产物中可能会混有苯磺酸 |
| C、装置③:实验室中可用此装置来分离含碘的四氯化碳液体,最终在锥型瓶中可获得碘 |
| D、装置④:实验室中可用此装置来制备乙酸乙酯并在烧瓶中获得产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在容积均为500mL的I、Ⅱ、Ⅲ三个密闭容器中分别充入l molN2和2.5molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下发生反应N2(g)+3H2(g)?2NH3(g)△H<O.实验测得反应均进行到t min时N2的体积分数如图所示.下列说法正确的是( )
在容积均为500mL的I、Ⅱ、Ⅲ三个密闭容器中分别充入l molN2和2.5molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下发生反应N2(g)+3H2(g)?2NH3(g)△H<O.实验测得反应均进行到t min时N2的体积分数如图所示.下列说法正确的是( )| A、当v(H2)=3v(N2)时,可以说明三个容器中的反应达平衡状态 |
| B、在t min时,一定达化学平衡状态的是Ⅱ和Ⅲ |
| C、在t min时,一定没有达化学平衡状态的是I |
| D、三个容器中的反应均达到平衡后,容器I中混合气体的平均相对分子质量最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量 | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 3.5 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com