

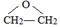 ;
; .
. 分析 乙烯与溴发生加成反应生成X为BrCH2CH2Br,X发生水解反应得到乙二醇,乙烯与过氧化氢发生加成反应生乙二醇,乙烯氧化生成Y,Y与水反应生成乙二醇,则Y为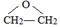 .乙二醇氧化生成乙二醛,乙二醛氧化生成乙二酸,乙二酸与乙二醇发生酯化反应生成环酯G为
.乙二醇氧化生成乙二醛,乙二醛氧化生成乙二酸,乙二酸与乙二醇发生酯化反应生成环酯G为 .
.
解答 解:乙烯与溴发生加成反应生成X为BrCH2CH2Br,X发生水解反应得到乙二醇,乙烯与过氧化氢发生加成反应生乙二醇,乙烯氧化生成Y,Y与水反应生成乙二醇,则Y为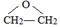 .乙二醇氧化生成乙二醛,乙二醛氧化生成乙二酸,乙二酸与乙二醇发生酯化反应生成环酯G为
.乙二醇氧化生成乙二醛,乙二醛氧化生成乙二酸,乙二酸与乙二醇发生酯化反应生成环酯G为 .
.
(1)Y的结构简式为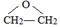 ,故答案为:
,故答案为: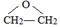 ;
;
(2)X为BrCH2CH2Br,化学名称是:1,2-二溴乙烷,故答案为:1,2-二溴乙烷;
(3)步骤Ⅲ的反应类型为酯化反应或取代反应,故答案为:酯化反应或取代反应;
(4)生成有机物G的化学反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,注意把握有机物的官能团的结构和性质,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
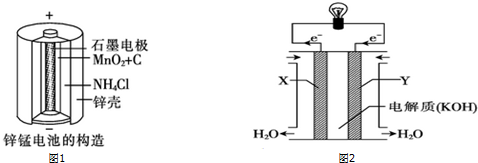
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
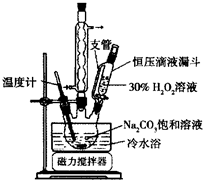 2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
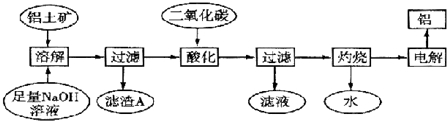
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCHCl3中含有碳氯键数目为0.3NA | |
| B. | 25℃时,0.1mol/L的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 1molNa2O和1molNa2O2的混合物中,含有的离子总数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 屠呦呦女士利用乙醚萃取青蒿素获得了2015年度诺贝尔生理学或医学奖,为人类防治疟疾作出了重大贡献 | |
| B. | 燃放烟花炮竹会加剧“雾霾”的形成,当“雾霾”中粉尘颗粒直径小于2.5 μm时,可能发生丁达尔效应 | |
| C. | 陶瓷、水泥、玻璃、大理石属于硅酸盐产品 | |
| D. | 光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
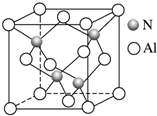 某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.
某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
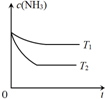 氨是一种重要的化工产品.
氨是一种重要的化工产品.| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com