
��12�֣�Na2S2O3���׳Ʊ��շۣ���ҽҩ��ӡȾ��Ӧ�ù㷺����ͨ�����з����Ʊ���ȡ15.1 gNa2SO3����80.0 mLˮ����ȡ5.0 g��ۣ��������Ҵ���ʪ��ӵ�������Һ�С�С��������У���Ӧ1Сʱ����ˡ���Һ��100�澭������Ũ������ȴ��10�������Na2S2O3��5H2O��
��1�������������Ҵ���ʪ��Ŀ���� ��
��2����Һ�г�Na2S2O3�Ϳ���δ��Ӧ��ȫ��Na2SO3�⣬����ܴ��ڵ��������������� ������ķ����ǣ�ȡ��������Һ�������������Ժ��˳�ȥS���ټ�BaCl2��Һ�����������ᷢ��������Ӧ�Ļ�ѧ����ʽΪ��
Na2SO3+2HCl=SO2��+H2O+2NaCl�� ��
��3��ij�������С���ú�0.100 mol��L-1Na2S2O3��Һ[��������Na2SO3����n(Na2S2O3) ��n(Na2SO3)
= 5��1]�ⶨij������ˮ��Ba2+��Ũ�ȡ�����ȡ��ˮ50.0 mL�������ʵ�����ȼ���������K2Cr2O7��Һ����BaCrO4������������ϴ�ӡ����˺���������ϡ�����ܽ⣬��ʱCrO42-ȫ��ת��ΪCr2O72-���ټӹ���KI��Һ����ַ�Ӧ��������Na2S2O3��Һ���еζ�����Ӧ��ȫʱ���������Na2S2O3��Һ�����Ϊ36.0 mL��
����֪�йط�Ӧ�����ӷ���ʽΪ����Cr2O72-+6I-+14H+ 2Cr3++3I2+7H2O��
��I2+2S2O32- 2I-+S4O62-����I2+SO32-+H2O 2I-+SO42-+2H+��
��ζ������п��� ��ָʾ��������ù�����ˮ��Ba2+�����ʵ���Ũ�ȡ�
��12�֡�
��1����������ۺ�Na2SO3��Һ��ֽӴ����ӿ췴Ӧ���ʣ�2�֣�
��2��Na2SO4��1�֣��� Na2S2O3+2HCl=S��+SO2��+H2O+2NaCl��2�֣�
��3�����ۣ�1�֣�
n(Na2S2O3) = 0.0360 L��0.100 mol��L-1 = 0.0036 mol
��n(Na2SO3) = 0.00360 mol��5 = 0.00072 mol
�������⣺2BaCrO4 ~ Cr2O72- ~ 3I2 ~ 6S2O32-
��n1(BaCrO4) = 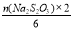 =
=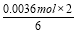 = 0.0012 mol
= 0.0012 mol
2BaCrO4 ~ Cr2O72- ~ 3I2 ~ 3SO32-
��n2(BaCrO4) = 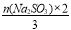 =
=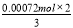 = 0.00048 mol
= 0.00048 mol
��c(Ba2+) = 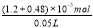 = 3.36��10-2 mol��L-1 ��6�֣�
= 3.36��10-2 mol��L-1 ��6�֣�
��������
�����������1�����������л��ܼ����Ҵ�������ˮ���������Ҵ���ʪ��ۣ�Ŀ������������ˮ�ĽӴ��������������Na2SO3��Һ��ֽӴ����ӿ췴Ӧ���ʣ�
��2�����������ڼ��ȵĹ����п��ܱ����������������ƣ���������ܴ��ڵ���������������Na2SO4�������� �Ȼ�����Һ���飬����������Ԫ�ط�Ӧ֪���������������壬��Na2S2O3�����ᷴӦ���ж����������ɣ������������ɣ����Ը�������IJ�ͬ���Լ�⣬�������һ���õĻ�ѧ����ʽΪNa2S2O3+2HCl=S��+SO2��+H2O+2NaCl��
��3��Na2S2O3��Һ���еζ����ǵⵥ�ʣ�����ѡ�õ�����ָʾ����������۵Ļ��ҺΪ��ɫ���ζ��յ�ʱ��ɫ��ʧ������Na2S2O3��Һ������ɼ���ⵥ�ʵ����ʵ������Ӷ��ɼ���BaCrO4���������ʵ�����Ҳ�Ϳ��Լ��㱵���ӵ�Ũ�ȣ����ݷ���ʽ�ó���ϵʽ�����岽����𰸡�
���㣺����������Ʊ��ķ�������ϵʽ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������������
A����ϩ�ͱ�����ʹ��ˮ��ɫ����ɫ��ԭ����ͬ
B�����ۡ���֬�������ʶ���ˮ�⣬��ˮ����ﲻͬ
C��ú�Ϳ���ʯ�ͷ����ã�������ȼ�Ϻͱ�������������
D���Ҵ������ᡢ�����������ܷ���ȡ����Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�߶���ѧ�ڽβ���5�� ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���г�������ȷ�����������ϵ����
ѡ�� | ������ | ������ |
A | H2O2��SO2����ʹ���Ը��������ɫ | ǰ�߱��ֳ���ԭ�Ժ��߱��ֳ�Ư���� |
B | �����������ڿ����н����䰵 | �����˻�ѧ��ʴ |
C | SiO2��������ἰ�Ӧ | SiO2������������ |
D | BaSO4������Һ�м��뱥��Na2CO3��Һ�а�ɫ���� | ˵��Ksp(BaSO4)����Ksp(BaCO3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ��װ���ڳ����¹�������Һ����仯���Բ��ƣ����պ�K�����ݷ��⡣���������в���ȷ����
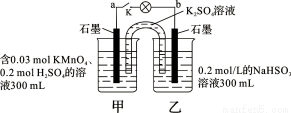
A������·����1.204��1022������ת��ʱ�����ձ�����Һ��pHԼΪ1
B����ع���ʱ�������е�K+������ձ������·�ĵ��ӷ����Ǵ�b��a
C����ع���ʱ�����ձ�����ˮ�������c(H+)��С
D���ҳ��е���������ΪSO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ���������ȷ����
A���Ǽ�����CH2OH���ͼ�������CH3O���������������
B��S2���Ľṹʾ��ͼ��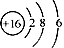
C������ȩ��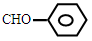
D��������Ϊ53��������Ϊ78�ĵ�ԭ�ӣ�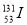
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й���Һ���Ʋ�������ҺŨ�ȵ�Ӱ���ԭ���������ȷ����
ѡ�� | ��Һ���Ʋ��� | Ӱ�� | ԭ����� |
A | ��2 g I2���뵽98 mL CCl4���ܽ���Ⱥ�����������Ϊ2%��I2��CCl4��Һ | ƫС | CCl4���ܶ� ����1 g/mL |
B | ����һ��Ũ�ȵ���Һʱ�����ձ��е���Һת�Ƶ�����ƿʱ������������ƿ�� | ƫС | ��������Һ�к������� |
C | ����һ�����ʵ���Ũ�ȵ�������Һ������ʱ�����ˮ�����˿̶��ߣ������õι����������ˮ����ҡ�� | ��Ӱ�� | �����˶��� ��ˮ |
D | ����һ�����ʵ���Ũ�ȵ�ʳ����Һ�����ݣ�ҡ�Ⱥ���Һ����ڿ̶��� | ƫ�� | Һ������ ƫС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����a��b��c��d��Ϊ��ѧ��ѧ�еij������ʻ������֮���ת����ϵ����ͼ��ʾ�����ֲ�������ȥ�������и��������У�ͨ��һ����Ӧ����ʵ��ͼʾת������

ѡ�� | a | b | c | d |
A | SO2 | SO3 | S | H2SO4 |
B | Na2O | Na2O2 | Na | NaOH |
C | CO | CO2 | C | H2CO3 |
D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���������ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����(����)
A�� �ڰ�ˮ�м���������ˮ���Ȼ�粒������ʹ��Һ�е�c(OH��)��С
B�� ��ӦHg(l)��H2SO4(aq)===HgSO4(aq)��H2(g)�ڳ����²����Է����У���H<0
C�� ��ҵ���ʳ��ˮ�У����ر������ӽ���Ĥ���������Һ������ң�Ŀ���DZ��������������������ռӦ
D�� �ڵ�Ũ�ȵ�NaCl��Na2CrO4ϡ��Һ�еμ�AgNO3��Һ��������AgCl��������Ksp(AgCl)<Ksp(Ag2CrO4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ������������ȷ����
A��0.5 L 1 mol/L NaHS��Һ�У�N(Na+)+N(HS��)=NA
B��12.4 g���ף�����ʽΪP4���к���P��P���ۼ�0.6 NA
C�������£�pH��2�Ĵ�����Һ�������е�H����Ϊ0.01 NA
D����92 g N2O4������������У��ָ������³�ѹʱ���������������ΪNA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com