
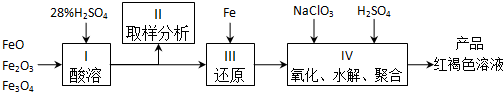
分析 铁的氧化物溶解于硫酸中取样分析溶液中的Fe2+、Fe3+的含量,因为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+先被还原为Fe2+;所以确定下一步还原所需铁的量,再被氧化为Fe3+;需要确定氧化Fe2+所需NaClO3的量,通过氧化、水解、聚合得到产品,
(1)根据配制一定量分数溶液的步骤:计算、称量、溶解,确定所用的仪器;
(2)为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+,然后Fe2+再被氧化Fe3+;
(3)从环保和成本方面考虑;
(4)根据将SO42?与Fe3+都采用沉淀法加以测定;
(5)根据测定Fe2O3来测定Fe3+的物质的量,根据测定 BaSO4的质量来测定SO42?的物质的量考虑;
(6)根据测定沉淀的质量分析基本步骤,从溶液中获得沉淀,要先过滤、洗涤,烘干,冷却再称量沉淀质量,根据沉淀质量再进行计算即可.
解答 解:(1)配制一定量质量分数硫酸溶液需要的仪器有:胶头滴管、量筒、玻璃棒、烧杯,故选b,故答案为:b;
(2)因为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+,所以确定下一步还原所需铁的量,然后Fe2+再被氧化Fe3+,需要确定氧化Fe2+所需NaClO3的量.
故答案为:bc;
(3)从环保和成本方面考虑,利是原料成本较低,弊是产生气体对大气有污染;
故答案为:原料成本低,产生的气体对大气有污染;
(4)因SO42?与Fe3+都采用沉淀法加以测定,测定硫酸根离子需要氯化钡,测定铁离子需要氢氧化钠,故答案为:ac;
(5)根据测定BaSO4的质量来测定SO42?的物质的量,根据氧化铁的质量结合元素守恒计算铁离子的物质的量,所以需要测定物质质量的物质为:Fe2O3、BaSO4,
故答案为:Fe2O3、BaSO4;
(6)测定聚合硫酸铁溶液中SO42-与Fe3+物质的量的原理:先后加入氯化钡、氢氧化钠并过滤,得到的沉淀先后洗涤,然后进行烘干或是灼烧,冷却,最后称量得到的固体的量即可,所以顺序是:bed,
故答案为:bed.
点评 本题以铁及其化合物为载体,以流程图形式考查了氧化还原反应知识、元素化合物的知识,注意溶液配制方法和步骤,测定物质含量的实验刚才分析判断,题目难度中等.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化产物与还原产物分子个数之比为15:1 | |
| B. | 氧化剂和还原剂是同一物质 | |
| C. | 反应过程中转移1mol电子,则产生2.24L气体(标准状况) | |
| D. | NaN3中氮元素的化合价为-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
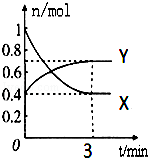 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4g)(无色),如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
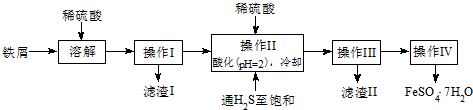
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.| 化学键 | N-N | N=N | N≡N | N-H | H-H |
| 键能/kJ•mol-1 | 159 | 418 | 946 | 391 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com