
【题目】钠露置在空气中,其变质结果产生的物质是
A. Na2O B. Na2CO3
C. NaHCO3 D. Na2O2
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是
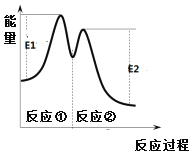
A. 0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B. Fe3+的作用是加快过氧化氢的分解速率
C. 反应①是吸热反应、反应②是放热反应
D. 反应2H2O2(aq)![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业上以NH3、CO2为原料生产尿素[CO(NH2)2],该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:___________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:
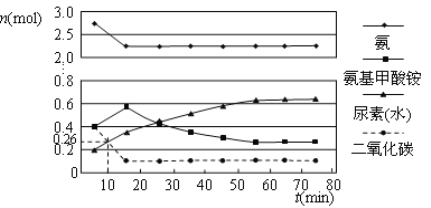
已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
Ⅱ.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种。
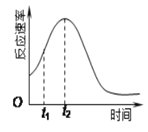
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
(3)猜想Ⅱ可能是:______________________
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
加入试剂 | 2mL0.1mol/L H2C2O4溶液、1mL 0.05mol/L 酸性KMnO4 | 2mL0.1mol/L H2C2O4溶液、 1mL 0.05mol/L 酸性KMnO4, 少量_______固体 |
实验现象 | 褪色时间10min | 褪色时间____10min (选填“<” “>”或 “=”) |
结论 | 猜想Ⅱ正确 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如水合物法、电渗透法、离子交换法和压渗法等.下列方法中也可以用来进行海水淡化的是( )
A.过滤法
B.蒸馏法
C.萃取法
D.结晶法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池的原理如图所示:回答下列问题 
(1)反应时电子从极流出(填a 或b )
(2)若电解质溶液为H2SO4溶液,则正极的电极反应式为 , 电池工作一段时间后,电解质溶液的酸性将会(填“增强”、“减弱”或“不变”)
(3)若电解质溶液为KOH溶液,则负极的电极反应式为 .
(4)电池工作时若转移4mol电子,则理论上需通入标况下的氢气L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体脑内有松果体腺,能分泌一种具有调节睡眠作用的物质,它的分泌量的大小随时间、光线、昼夜变化等条件的不同而变化,比如晚上分泌得多,白天分泌得少。这种物质叫松果体素,又叫褪黑素,也就是保健市场上出售的“脑白金”。脑白金的有效成分的结构简式如图所示,下列对该化合物的叙述正确的是 ( )
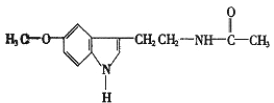
A. 它属于氨基酸
B. 它属于高分子化合物
C. 分子式为C13N2H14O2
D. 在一定条件下可以发生加成反应和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计了三个实验方案,用以检验淀粉的水解情况。
方案甲:淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 溶液变蓝。
溶液变蓝。
结论:淀粉完全没有水解。
方案乙:淀粉液![]() 水解液
水解液![]() 无银镜现象。
无银镜现象。
结论:淀粉完全没有水解。
方案丙:淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 有银镜现象。
有银镜现象。
结论:淀粉已经水解。
(1)淀粉的水解产物是______________________(填名称)。利用它的________________(填还原性或氧化性)可进行检验。
(2)方案甲结论不正确,正确结论应为淀粉可能完全没有水解或______________________________。
(3)方案乙结论也不正确,淀粉也可能部分或完全水解,因为__________________________________。
(4)方案丙的结论是正确的,其中最后一步的银氨溶液也可换成新制氢氧化铜悬浊液,则加热反应现象为_______________________________。
(5)若想进一步检验方案丙中淀粉是否完全水解,应取少量中和液,加______________,若现象为溶液变蓝,则证明淀粉__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 浓盐酸与铁屑反应:2Fe + 6H+= 2Fe3+ + 3H2↑
B. 往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4+ + OH-=NH3↑ + H2O
C. 往酸性碘化钾溶液中滴加适量的双氧水:2I- + 2H+ + H2O2 =I2 + 2H2O
D. HS-的电离:HS- + H2O = H3O+ + S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( ) 
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:Y>X
D.X,Z形成的化合物中只有离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com