
| 族 周期 | IA | | 0 | |||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | | | | | | ② | ③ | |
| 3 | ④ | ⑤ | | | | ⑥ | ⑦ | ⑧ |
| | 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | ||||
| 第一组 | 1 | 40 | FeCl3溶液 | 快速产生大量气泡 | 相同条件下,温度升高,化学反应速率加快 |
| 2 | 20 | A | 缓慢产生适量气泡 | ||
| 3 | 5 | FeCl3溶液 | 缓慢产生极少量气泡 | ||
| 第二组 | 4 | t | MnO2 | 快速产生大量气泡 | |
| 5 | 20 | 无 | 缓慢产生极少量气泡 | ||
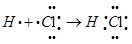 (3)Na>S>F (4)①温度 ②FeCl3溶液 ③20
(3)Na>S>F (4)①温度 ②FeCl3溶液 ③20 ⑤在20℃(或相同条件下),MnO2可以加快H2O2分解的反应速率。
⑤在20℃(或相同条件下),MnO2可以加快H2O2分解的反应速率。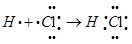 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| 元素化合物的性质 |  | 形成常见的两性氧化物 | Z2是常见保护气 | W3可用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.14N与15N为同种核素 |
| B.14N的第一电离能小于14C |
| C.15NH3与14NH3均能形成分子间氢键 |
| D.CH315NH2与CH3CH214NH2互为同系物 |
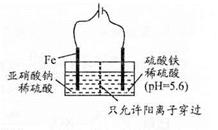
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 mol电子,写出相应反应的化学方程式_______。
mol电子,写出相应反应的化学方程式_______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.同一主族的元素,原子半径越大,氧化性越强 |
| C.ⅦA族元素形成的单质,其熔点随元素原子序数增大而降低 |
| D.从上到下,ⅦA族元素形成的氢化物稳定性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 -NMR(核磁共振)可以用于含碳化合物的结构分析。
-NMR(核磁共振)可以用于含碳化合物的结构分析。 表示的碳原子
表示的碳原子| A.核外有13个电子,其中4个能参与成键 |
| B.核内有6个质子,核外有7个电子 |
| C.质量数为13,原子序数为6,核内有7个质子 |
| D.质量数为13,原子序数为6,核内有7个中子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| D.Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com