
| A. | N2 | B. | NO2 | C. | NH3 | D. | NO |
分析 X、Y、Z、W(含同一元素),其中X能经过两步氧得Z,Z再与水反应可以生成对应的酸或碱,则X可以含有C、N、S、Na等元素,X能与W发生反应生成一种易溶于水的盐,符合此条件的X只能为NH3,据此解答.
解答 解:A.氮气氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水生成硝酸,硝酸与氮气不反应,故A错误;
B.二氧化氮中氮元素为+4价,不能连续氧化,故B错误;
C.NH3能与氧气生成NO,NO再与氧气反应生成NO2,NO2与水反应生成HNO3,HNO3与NH3反应生成NH4NO3,NH4NO3是一种易溶于水的盐,故C正确;
D.一氧化氮氧化生成二氧化氮,二氧化氮氧化生成五氧化二氮,五氧化二氮与水反应生成硝酸,但是硝酸与一氧化氮不反应,故D错误;
故选:C.
点评 本题考查了物质间的转化,熟悉各物质的性质和发生的反应是解题关键,注意对相关知识的积累,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | m=Vρa% | B. | c=1000ρaM | C. | c=$\frac{1000m}{VM}$ | D. | a%=$\frac{cM}{1000ρ}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硅酸钠溶液中通入少量CO2气体 SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| B. | 将Cu片插入FeCl3溶液中 Cu+Fe3+═Fe2++Cu2+ | |
| C. | 向烧碱溶液中滴加少量Al2(SO4)3溶液 Al3++4OH-═[Al(OH)4]- | |
| D. | 将Ag丝插入NaNO3和H2SO4的混合液中 3Ag+4H++NO3-═3Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHA溶液一定呈酸性 | B. | c(H+)•c(OH-)=1×10-14x | ||
| C. | c(Na+)=c(K+) | D. | c(Na+)+c(K+)=0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
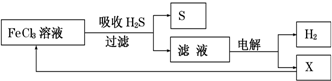
| A. | 吸收H2S的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+ | |
| B. | 电解时选用阴离子交换膜,电解过程中的阳极区反应主要为:2Cl--2e-=Cl2 | |
| C. | 电解过程中若阴极产生2.24L气体,则阳极区产生0.2mol Fe3+ | |
| D. | 实验室可用点燃充分燃烧的方法消除H2S污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量浓度的溶液,定容时俯视刻度线 | |
| B. | 测量一包固体的质量,将药品放在右盘,砝码放在左盘,并需移动游码使之平衡 | |
| C. | 中和滴定用的锥形瓶加入待测液后,再加少量蒸馏水稀释 | |
| D. | 在敞口容器中测量氢氧化钠和稀盐酸反应的中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
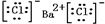 ,①中形成沉淀的离子方程式为SO42-+Ba2+=BaSO4↓;
,①中形成沉淀的离子方程式为SO42-+Ba2+=BaSO4↓;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B物质的相对分子质量 | D. | 气体的总物质的量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com