
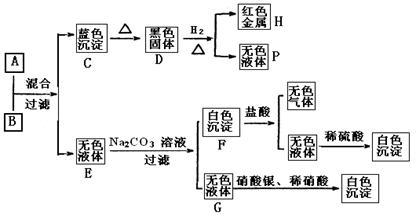
科目:高中化学 来源:不详 题型:填空题
| A | | | ||||||||||||||||
| | B | | | C | D | E | F | | ||||||||||
| G | H | I | J | | L | K | M | |||||||||||
| | | | | | | | N | | | Q | | | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)
设计一个实验,不用实验室里的任何试剂,只用常用的仪器,区分B、Y两种物质(简要说明实验方法和实验结论)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
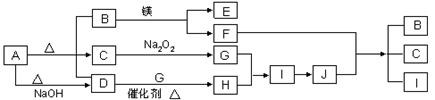
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. (A-N+m)mol (A-N+m)mol | B. (A-N)mol (A-N)mol |
C. (A-N)mol (A-N)mol | D. (A-N+m)mol (A-N+m)mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2的水溶液能够导电,但SO2是非电解质 |
| B.饱和氯水的导电性很好,所以氯气是强电解质 |
C. 和 和 为不同的核素,二者核外电子数不同 为不同的核素,二者核外电子数不同 |
| D.化合反应和分解反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可与活泼金属直接发生化学反应 | B.易溶于水也易溶于NaOH溶液 |
| C.是一种有毒气体 | D.可用HCN溶液与MnO2混合加热制取 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com