
����Ŀ���������ƣ�NaNO2����һ����Ҫ�Ĺ�ҵ�Σ�Ҳ���������ࡢ�����ʳƷ��Ⱦɫ�ͷ�����������ˮ�������Ҵ�. ij��ѧ��ȤС����������ƽ��ж�Ƕ�̽����
i.�������Ƶ��Ʊ�
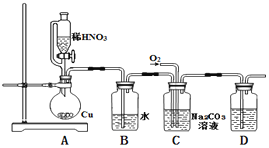
��1��ʵ�����ú�ѹ��Һ©���������ͨ��Һ©�����������ŵ���____��
��2��D�г���ʯ��ˮ����ǣ���C���Ʊ�NaNO2�����ӷ���ʽΪ_______________��
ii. ̽���������������ᷴӦ�������ɷ֣�
��֪����NO+NO2+2OH���T2NO2��+H2O ������Һ�����¶ȣ�NO2��21�棬NO����152��

��3����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪����Ŀ����___________��
��4��Ϊ�˼���װ��A�����ɵ�����������������˳����������ӣ���
A��C��______��______��______��
��5���ڹرյ��ɼУ���Һ©������������70%�����A�в�������ɫ���壮
��ȷ��A�в��������庬��NO�����ݵ�������_________________��
��װ��B��������____________________��
iii. ���ʵ��֤������������NaNO2���������ԣ�___________��
��ѡ�õ��Լ���NaNO2��Һ��KMnO4��Һ��FeSO4��Һ��KI��Һ��ϡ���ᡢ������Һ��KSCN��Һ
���𰸡� ƽ���Һ©������ƿ��ѹǿ�������������� 4NO+O2+2CO32-=4NO2-+2CO2 �ž�װ���п�������ֹ���ɵ�NO�����������Ų�������ļ��� E D B D��ͨ����������������ɫ��Ϊ����ɫ β�����������յ��������ֹ������Ⱦ ȡ����������Һ���μ�ϡ�����ữ���μӼ���KSCN��Һ����Һ��Ϊdz��ɫ���μ�����NaNO2��Һ����ʱ��Һ��dz��ɫ��ΪѪ��ɫ��֤��NaNO2����������;����ȡ�⻯����Һ���μ�ϡ�����ữ���μӵ�����Һ�����������μ�����NaNO2��Һ����Һ������֤��NaNO2����������
����������1����ѹ��Һ©����������ѹǿ��ȣ���������ͨ��Һ©�����������ŵ���ƽ���Һ©������ƿ��ѹǿ�������������£���2��D�г���ʯ��ˮ����ǣ�˵���ж�����̼���ɣ���Ӧ����NO��������̼���ƣ���C���Ʊ�NaNO2�����ӷ���ʽΪ4NO+O2+2CO32-=4NO2-+2CO2��
��3��NO�����ױ�����������װ�����п�������������NO���ɣ�����ͨ������Ŀ�����ž�����װ���еĿ�������ֹ������NO����������NO2����4��C����ˮ������Bβ����������ֹ��Ⱦ������D����NO��E��ȴ������������������NO������װ�õ�����ΪA��C��E��D��B����5����D����ɫ�����ɺ�ɫ��˵������NO���壬���ȷ��A�в��������庬��NO�����ݵ�������D��ͨ����������������ɫ��Ϊ����ɫ���ڸ������Ϸ�����֪װ��B��������β�����������յ��������ֹ������Ⱦ����6�������������������⻯�����ɵ��ʵ⣬������������ɫ����ʵ�鷽���ǣ�ȡ�⻯����Һ���μ�ϡ�����ữ���μӵ�����Һ�����������μ�����NaNO2��Һ����Һ������֤��NaNO2���������ԣ�����ȡ����������Һ���μ�ϡ�����ữ���μӼ���KSCN��Һ����Һ��Ϊdz��ɫ���μ�����NaNO2��Һ����ʱ��Һ��dz��ɫ��ΪѪ��ɫ��֤��NaNO2���������ԡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����״���£�3.4gNH3��________LCO���������е�������ͬ��
��2��0.2L0.5mol��L��1Al2(SO4)3��Һ��0.5L0.5mol��L��1Na2SO4��Һ������SO42������Ũ��֮��Ϊ_________��
��3����״������NH3 �� CH4 ��ɵĻ�������ƽ���ܶ�Ϊ 0.75g/L���� NH3 ���������Ϊ__________
��4������ 100mL 2mol/L �� H2SO4 ��Һ��ȡ���ƺ����Һ 20mL������������п�����ɱ���� ���������Ϊ_____L��
��5����֪ 16g A �� 20g B ǡ����ȫ��Ӧ���� 0.04mol C �� 32g D���� C ��Ħ������Ϊ______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�������鶼�ܷ���ȡ����Ӧ
B.ʯ�͵ķ����ú�ĸ����ǻ�ѧ�仯
C.��ҵ�Ͽ�ͨ��ʯ�ͷ���ֱ�ӵõ����顢��ϩ�ͱ�
D.��ϩ�;���ϩ����ʹ������Ȼ�̼��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������֬�����벻����ȩͪ(��ϩȩ��Ȳͪ��)��±����������Ӧ��

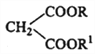 + R3Cl
+ R3Cl 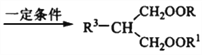 +HCl
+HCl
�л�������H�ĺϳ�·�����£�
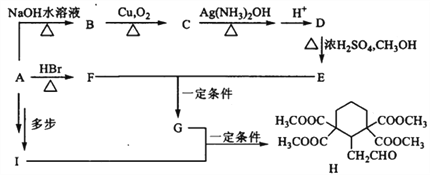
��1��A�ķ���ʽΪC3H7OBr���˴Ź���������ʾ����������壬�������1��2��2��2,д��A�к�������������______________��F��ϵͳ������_______________��
��2���ڼ��������£�C����������������ͭ����Һ��Ӧ�Ļ�ѧ����ʽ�ǣ�____________��
��3��B��D��1��1�γɵĸ߷��ӻ�����Ľṹ��ʽΪ_____________________________________��
��4��E��F��1��1��Ӧʱ�õ�J(C8H12O4)��J�Ľṹ��ʽΪ___________________________________��
��5����֪G�ķ���ʽΪC13H20O8��д��ͬʱ��������������G��ͬ���칹����____________��
����ˮ��õ�4���Ӽ״�;����һ�ȴ����������
��6����ֻ��C��H��O,�����ķ���ʽΪ____________�������м���������ˮ��������ˮ��ɫ�����ⲻ��˵�����к��в�����̼̼����ԭ����_________________��
��7����A���ಽ��Ӧ�Ƶ�����д���ϳ�·��______________(�����Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊά������ѪҺ�е�Ѫ�Ǻ������ڸ�������Һʱ��ͨ����������ע��Һ����ͼ��ҽԺ������Һʹ�õ�һƿ��������Ϊ5%�������ǣ�C6H12O6��ע��Һ��ǩ��������۲��ǩ���������ݺ���ʽ���㣨Ҫ��д�������������

��1������Һ�����ʵ���Ũ��Ϊ_________ mol��L��1���������2λ��Ч���֣���
��2������Һ���ܶ�Ϊ__________ g��mL��1��
��3������Ӹ�ƿ��ȡ��75g������ע��Һ�������Ϊ15%��ע��Һ����Ҫ����______g�����ǹ��壨������ȷ��0.1g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ�������м��к����ж�Ӧ�������������һ�������ʵ���Ũ�ȹ�ʽ����
��� | �� | �� | �� | �� | �� |
�� | �������� | ��״���� ����Ħ����� | ����Na2SO4������ | ����KCl�� �������� | �DZ�״�� �����ʵ����� |
�� | �����ӵ����� | ��״���� �����ܶ� | ��Һ����� | ��Һ���ܶ� | ���ʵ�Ħ������ |
A. �٢ڢ� B. �٢��ܢ� C. �ۢ� D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ�����������˵����ȷ����( )
A. 46gNO2��N2O4�Ļ��Һ����ԭ����Ϊ3NA
B. 4��ʱ9mLˮ��11.2L����������ͬ�ķ�����
C. ͬ��ͬѹ�£�NA��CO2��NA��N2��O2�Ļ���������������
D. 1.01��105Paʱ��11.2 L����������ԭ����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���H���ṹ��ʽΪ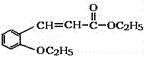 ���Ǻϳɸ߷��ӻ�����M�ĵ��壬H����ͨ���л���A������ʽΪC7H8O���ͱ�ͪΪԭ�������кϳɣ���ϳ�·�����£�
���Ǻϳɸ߷��ӻ�����M�ĵ��壬H����ͨ���л���A������ʽΪC7H8O���ͱ�ͪΪԭ�������кϳɣ���ϳ�·�����£�
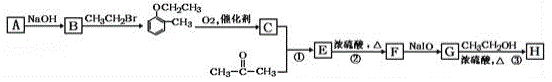
��֪����![]()
��
��ش��������⣺
��1��A�Ļ�ѧ����Ϊ_______________��G�����������ŵ�������________________________���ٺ͢ڵķ�Ӧ���ͷֱ���______________��__________________��
��2�������л���A �й����ŵķ���Ϊ__________________________________��
��3���߷��ӻ�����M �Ľṹ��ʽΪ__________________��
��4����Ӧ�۵Ļ�ѧ��Ӧ����ʽΪ__________________________________��
��5���л���C �ж���ͬ���칹�壬�������ڷ����������ͬ���칹����___________�֡�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com