
在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O2===2NO,经测定前3 s用N2表示的反应速率为0.1 mol·L-1·s-1,则6 s末NO的浓度为
A.1.2 mol·L-1 B.大于1.2 mol·L-1
C.小于1.2 mol·L-1 D.不能确定
科目:高中化学 来源: 题型:
下列说法正确的是( )
①难溶电解质达到沉淀溶解平衡时,溶液中各种离子的溶解(或沉淀)速率都相等
②难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动
③向Na2SO4溶液中加入过量的BaCl2溶液,则SO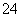 沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO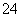
④Ksp小的物质其溶解能力一定比Ksp大的物质的溶解能力小
⑤为减少洗涤过程中固体的损耗,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀
⑥洗涤沉淀时,洗涤次数越多越好
A.①②③ B.①②③④⑤⑥
C.⑤ D.①⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
有关氨气和甲烷分子空间构型叙述正确的是( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化
B.NH3为三角锥形,甲烷是正四面体形
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较弱
D.NH3和CH4都是sp3型杂化,键角都是109°28′
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
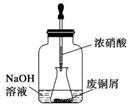
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式_____________________________________
________________________________________________________________________。
(2)上图装置中NaOH溶液的作用是__________________________________
________________________________________________________________________。
(3)步骤二中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外),水浴加热的优点是________________________________________________
________________________________________________________________________。
(4)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业尾气中的氮氧化物常用氨催化吸收法,原理是NH3和NOx反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
Ⅰ.提供的装置
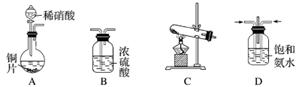

Ⅱ.NH3的制取
(1)下列有关实验室制备气体的说法正确的是________(填序号)。
①可以用排饱和食盐水的方法收集氯气 ②用赤热的炭与水蒸气反应制取氢气 ③实验室制氧气有时需要加热,有时不需要加热 ④用无水氯化钙干燥氨气 ⑤用浓盐酸洗涤高锰酸钾分解制氧气的试管
(2)从所提供的装置中选取一个能制取氨气的装置:__________________________(填字母)。
(3)当采用你所选用的装置制取氨气时,相应反应的化学方程式是________________________________________________________________________。
Ⅲ.模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
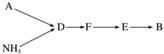
(4)A中反应的离子方程式为_______________________________________________
________________________________________________________________________。
(5)装置D的作用有:使气体混合均匀、调节气流速度,还有一个作用是________________________________________________________________________。
(6)D装置中的液体可换成________(填字母)。
a.CuSO4 b.H2O c.CCl4 d.浓硫酸
(7)该同学所设计的模拟尾气处理实验还存在的明显缺陷是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对反应A+BAB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol ②50 mL溶液中含A、B各0.05 mol ③0.1 mol·L-1的A、B溶液各10 mL④0.5 mol·L-1的A、B溶液各50 mL
四者反应速率的大小关系是( )
A.②>①>④>③ B.④>③>②>①
C.①>②>④>③ D.①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
COCl2的分解反应为COCl2(g)===Cl2(g)+CO(g) ΔH=+108 kJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10 min到14 min的COCl2浓度变化曲线未示出):

①计算反应在第8 min时的平衡常数K=__________;
②比较第2 min反应温度T(2)与第8 min反应温度T(8)的高低:T(2)________T(8)(填“<”、“>”或“=”);
③若12 min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=________mol·L-1;
④比较产物CO在2~3 min、5~6 min和12~13 min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小_____________________________;
⑤比较反应物COCl2在5~6 min和15~16 min时平均反应速率的大小:v(5~6)________v(15~16)(填“<”、“>”或“=”),原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应mA(g)+nB(g)pC(g)+qD(g)的v-t图像如图甲所示,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。
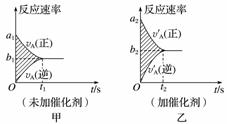
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2
⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧图Ⅱ中阴影部分面积更大
以上所述正确的为( )
A.②④⑤⑦ B.②④⑥⑧
C.②③⑤⑦ D.②③⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的锌粒与足量稀硫酸反应,向反应混合液中加入某些物质,下列判断正确的是( )
A.加入少量水,产生H2速率减小,H2体积不变
B.加入NH4HSO4固体,产生H2速率不变,H2体积不变
C.加入CH3COONa固体,产生H2速率减小,H2体积减小
D.滴加少量CuSO4溶液,产生H2速率变大,H2体积不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com