
| A. | 标准状况下,1mol 任何物质所占的体积都约为22.4L | |
| B. | 1mol 氖气和1mol氧气体积相同 | |
| C. | 标准状况下,6.02×1023个分子所占的体积约为22.4L | |
| D. | 标准状况下,1mol氧气和氮气的混合气体(任意比)的体积约为22.4L |
分析 A.气体摩尔体积只适用于气体;
B.相同条件下气体摩尔体积相同;
C.标况下,气体摩尔体积是22.4L/mol,气体摩尔体积仅适用于气体;
D.标况下,气体摩尔体积是22.4L/mol,1mol任何气体在标况下的体积约是22.4L.
解答 解:A.气体摩尔体积只适用于气体,标况下1mol任何气体体积都约是22.4L,但固体和液体体积要远远小于22.4L,故A错误;
B.温度和压强未知导致气体摩尔体积未知,所以无法计算二者体积相对大小,故B错误;
C.标况下,气体摩尔体积是22.4L/mol,气体摩尔体积仅适用于气体,6.02×1023个分子可能是固体或气体,如果是气体则其所占的体积约为22.4L,如果是固体和液体,其体积远远小于22.4L,故C错误;
D.标况下,气体摩尔体积是22.4L/mol,1mol任何气体在标况下的体积约是22.4L,所以标准状况下,1mol氧气和氮气的混合气体(任意比)的体积约为22.4L,故D正确;
故选D.
点评 本题考查物质的量有关计算,为高频考点,侧重考查气体摩尔体积有关计算,明确气体摩尔体积适用范围及适用条件是解本题关键,易错选项是BC.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe2+被H2S04氧化成Fe3+ | |
| B. | 原无色溶液中一定含有SCN- | |
| C. | Fe2+与SCN-不能形成红色化合物 | |
| D. | 将稀H2SO4换成新制氯水,混合液也会出现红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$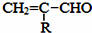
 的相对分子质量大2,则符合下列条件的G的同分异构体有3种.
的相对分子质量大2,则符合下列条件的G的同分异构体有3种. 的合成路线
的合成路线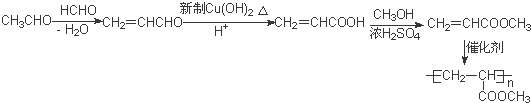 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com