
常温下,下列各组离子或分子在指定分散系中一定能大量共存的是
A.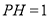 的溶液中:
的溶液中: 、
、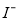 、
、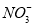 、
、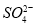
B.氢氧化铁胶体中: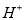 、
、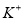 、
、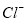 、
、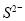
C.在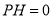 的溶液中:
的溶液中: 、
、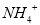 、
、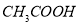 、
、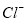
D.水电离产生的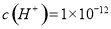
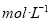 的溶液中HCO3-、
的溶液中HCO3-、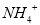 、
、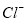 、
、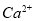
科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强
B.已知①Fe + Cu2+ = Fe2+ + Cu;② 2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为:Fe3+ > Cu2+ > Fe2+
C.已知还原性:B-> C-> D-,反应 2C-+ D2 = 2D-+C2和反应 2C-+ B2 = 2B-+C2都能发生
D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:选择题
等体积等浓度的稀硝酸与过量的下列物质充分反应放出NO,消耗下列固体的物质的量最少的是
A.FeO B.Fe C.Cu D.Ag
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:填空题
(14分)铜及其化合物在生产生活中有广泛应用,铜在化合物中的常见化合价有+1、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。
(1)工业上可用Cu2S+O2 2Cu+SO2反应制取粗铜,该反应中是 元素被还原 。
2Cu+SO2反应制取粗铜,该反应中是 元素被还原 。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为: 温度控制在50℃-60℃的原因除了加快反应速率外,还有 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式 。
(3)现向Cu、Cu2O和CuO组成的混合物中,加入2 L 0.6 mol·L-1 HNO3溶液恰好使混合物溶解,同时收集到4480 mL NO气体(标准状况)。Cu2O跟稀硝酸反应的离子方程式 。若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。若混合物中含0.2 mol Cu,将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是( )
A.两个反应中均为硫元素被氧化
B.碘元素在反应①中被还原,在反应②中被氧化
C.氧化性:MnO2>SO42->IO3->I2
D.反应①、②中生成等量的I2时转移电子数比为1:5
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.Na2O2是碱性氧化物,能与CO2、H2O反应作供氧剂
B.浓硫酸具有强氧化性,常温下可用铝罐盛装
C.SO2和Cl2均具有漂白性,两者混合使用可以增强漂白效果
D.氯气具有酸性,可与烧碱或石灰乳反应制取含氯消毒剂
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市诸城高三10月月考化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源和药物。下图是从海水中提取某些原料的流程图。
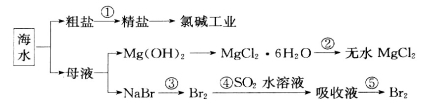
下列有关说法正确的是
A.从海水中提取物质都必须通过化学反应才能实现
B.第②步属于物理变化
C.从第④~⑤步的目的是浓缩、富集溴单质
D.第①步中除去粗盐中的SO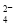 、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
第Ⅱ卷(非选择题,共55分)
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:填空题
(12分)某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数。
【方法一】测 SO2质量法
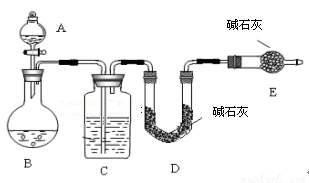
采用如图所示装置,通过实验测定生成SO2的质量。
(1)C中盛放的试剂是 ,E装置的作用是 。
(2)若实验前称取m1g样品,再测得SO2的质量为m2g,则可得Na2SO4质量分数,其中m2是通过测定 (填装置符号)装置在实验前后的质量差得到的。该方法的缺点是(只答一点)
。
【方法二】测沉淀质量法
第一步:称取m3g样品,置于小烧杯中 第二步:向小烧杯中加入足量稀盐酸,加热
第三步:再向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤 第四步:干燥沉淀,称重为m4g
(3)简述洗涤沉淀的方法: 。
(4)若m3=2m4 则试样中Na2SO4的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高三10月阶段测试化学试卷(解析版) 题型:选择题
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:
3NF3+5H2O=2NO+HNO3+9HF。下列有关说法正确的是( )
A.NF3是氧化剂,H2O是还原剂
B.若生成0.2 mol HNO3,则转移0.2 mol电子
C.还原剂与氧化剂的物质的量之比为2∶1
D.NF3在潮湿的空气中泄漏会产生红棕色气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com