
| A. | $\frac{3}{(m-n)}$mL | B. | $\frac{(m-n)}{3}$ mL | C. | $\frac{(4m-1)}{13}$ mL | D. | $\frac{(m-n)}{3}$3 mL |
分析 先根据反应3NO2+H2O=2HNO3+NO,求出所有的NO,再根据反应4NO+3O2+2H2O=4HNO3,求出剩余气体的体积.
解答 解:根据反应可知
3NO2 +H2O=2HNO3 +NO,
3 1
m $\frac{1}{3}$m
所以反应后NO气体共(n+$\frac{1}{3}$m)mL,
设消耗的氧气的体积为x,
由 4NO+3O2 +2H2O=4HNO3,
4 3
(n+$\frac{1}{3}$m) x
x=$\frac{3n+m}{4}$,
由m>n可知,x>$\frac{3n+m}{4}$=n,
显然氧气不足,完全反应,
剩余气体为NO,NO的体积为(n+$\frac{1}{3}$m)mL-$\frac{4}{3}$nmL=$\frac{m-n}{3}$mL,
故选B.
点评 本题考查氮的氧化物与水的反应,明确发生的化学反应及m、n的关系是解答本题的关键,注意体积与物质的量成正比,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
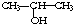 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2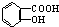 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备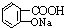
| A. | 只有①③④ | B. | 只有①④ | C. | 只有① | D. | 都不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
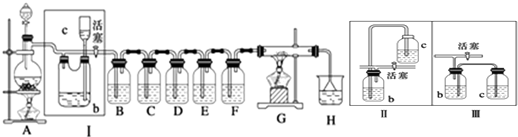
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L甲醛完全燃烧产生NA个CO2分子 | |
| B. | 1L1mol/L Na2CO3溶液中,阴离子个数等于NA | |
| C. | 100 g 98%的浓硫酸中含氧原子个数为4NA | |
| D. | 常温常压下,1mol白磷中含有共价键为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 离子方程式 |
| A | 向(NH4)2SO4溶液中加入足量Ba(OH)2溶液并加热 | 生成使湿润的红色石蕊试纸变蓝的气体 | NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
| B | 加热滴有酚酞的Na2CO3溶液 | 溶液红色加深 | CO32-+2H2O═H2CO3+2OH- |
| C | 用惰性电极电解氯化镁溶液 | 有白色沉淀和无色无味气体生成 | 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
| D | 向Na2S2O3溶液中加入稀硫酸 | 溶液出现浑浊,生成无色刺激性气味气体 | 2H++S2O32-═S↓+SO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | abdi | B. | cefk | C. | fghl | D. | bcegj |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com