
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量甘蔗渣,对甘蔗渣进行综合利用,可以提高经济效益,减少对环境的污染。如图所示为用甘蔗渣为原料制取各物质的转化过程图。
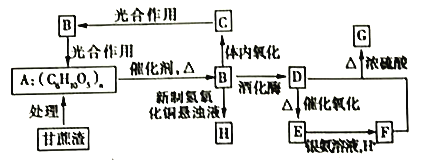
已知:①B在人体组织中发生缓慢氧化,放出热量,提供生命活动需要的能量。
②G是具有果香气味的液体,体积分数75%的D的水溶液常用于医疗消毒,并且可以代替汽油作汽车燃料。
③R—CHO![]() R—COOH
R—COOH
(1)A的化学名称为___________,B的分子式为___________。
(2)E的结构简式为___________,F分子中含有的官能团的名称为___________。
(3)D+F→G的化学方程式为___________,该反应的反应类型为___________。
【答案】纤维素 C6H12O6 CH3CHO 羧基 CH3COOH+C2H5OH![]() CH3COOCH2CH3+H2O 酯化反应(或取代反应)
CH3COOCH2CH3+H2O 酯化反应(或取代反应)
【解析】
A为甘蔗渣主要成分纤维素;B在人体组织中发生缓慢氧化,放出热量,提供生命活动需要的能量,所以B为葡萄糖;体积分数75%的D的水溶液常用于医疗消毒,并且可以代替汽油作汽车燃料,所以D为乙醇;D(乙醇)催化氧化生成E(乙醛);E(乙醛)氧化成F(乙酸);F(乙酸)与D(乙醇)酯化反应生成具有果香气味的液体G(乙酸乙酯)。
(1)A为甘蔗渣主要成分纤维素,B在人体组织中发生缓慢氧化,放出热量,提供生命活动需要的能量,所以B为葡萄糖,分子式为C6H12O6;
正确答案:纤维素;C6H12O6。
(2)D(乙醇)催化氧化生成E(乙醛),E结构简式为CH3CHO;E(乙醛)氧化成F(乙酸),乙酸分子中含有的官能团的名称为羧基;
正确答案:CH3CHO;羧基。
(3)F(乙酸)与D(乙醇)反应的化学方程式为CH3COOH+C2H5OH![]() CH3COOCH2CH3+H2O,该反应的反应类型为酯化反应(或取代反应);
CH3COOCH2CH3+H2O,该反应的反应类型为酯化反应(或取代反应);
正确答案:CH3COOH+C2H5OH![]() CH3COOCH2CH3+H2O;酯化反应(或取代反应)。
CH3COOCH2CH3+H2O;酯化反应(或取代反应)。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,按要求完成各小题。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)元素①的元素符号:_______________
(2)元素⑧的单质电子式_______________
(3)元素⑤的原子结构示意图______________
(4)化学性质最不活泼的元素______(填元素符号,下同),非金属性最强的元素是________。金属性最强的单质_______。
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的 _____(填化学式,下同)。①③⑤三种元素的原子半径由大到小的顺序为_____________。
(6)某元素的最高价氧物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为 _____,与氢氧化钠溶液反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中含酚废水中有机物可用C6H5OH表示,左、中、右室间分别以离子交换膜分隔。下列说法错误的是
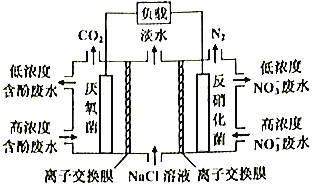
A. 左室电极为该电池的负极
B. 右室电极反应式可表示为:2NO3-+10e-+12H+=N2↑+6H2O
C. 左室电极附近溶液的pH增大
D. 工作时中间室的Cl-移向左室,Na+移向右室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将AgCl分别加入盛有:①5 mL水;② 6 mL0.5mol·L-1 NaCl溶液;③10 mL0.2mol·L-1 CaCl2溶液;④50 mL0.1mol·L-1盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是
A. ④③②① B. ②③④① C. ①④③② D. ①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为以Pt为电极的氢氧燃料电池的工作原理示意图,稀H2SO4溶液为电解质溶液。下列有关说法不正确的是

A. a极为负极,电子由a极经外电路流向b极
B. a极的电极反应式:H2-2e-===2H+
C. 电池工作一段时间后,装置中c(H2SO4)增大
D. 若将H2改为CH4,消耗等物质的量的CH4时,O2的用量增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,电子转移发生在不同物质的同种元素之间的是
A. 2H2S+SO2=3S↓+2H2OB. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C. 2KClO3![]() 2KCl+3O2↑D. CuO+H2SO4=CuSO4+H2O
2KCl+3O2↑D. CuO+H2SO4=CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“变废为宝”是化工的重要主题。工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有CuCl2,FeCl2等)制备碱式碳酸铜Cu2(OH)2CO3],其制备过程如下图所示:
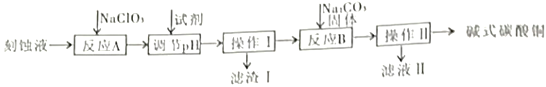
查阅资料得知,一定浓度的Cu2+、Fe2+、Fe3+生成氢氧化物沉淀的pH如下表:
金属离子 | Cu2+ | Fe2+ | Fe3+ |
开始沉淀的pH | 4.2 | 6.5 | 1.4 |
沉淀完全的pH | 6.7 | 9.7 | 3.7 |
(1)电子工业中用FeCl3溶液制作铜制印刷电路板,该反应的离子方程式为___________。
(2)操作I、操作Ⅱ所用的玻璃仪器除烧杯外还需要______________________。
(3)氯酸钠的作用是____________________________________________;反应A中氧化剂与还原剂物质的量之比是___________。
(4)调节pH的范围为___________,可以选择的试剂是___________(填序号)。
A.氨水 B.硫酸铜 C.氧化铜 D.氢氧化铜
(5)已知滤液Ⅱ中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:___________。
(6)若废液中CuCl2的含量为13.5%,则1吨废液理论上可提炼碱式碳酸铜________吨。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、NO、CO污染物处理,对建设美丽中国具有重要意义。
(1)①NO2(g)+CO(g)==CO2(g)+NO(g)△H1=-234.00kJ/mol
②1/2N2(g)+1/2O2(g)=NO(g)△H2=-89.75kJ/mol
③2NO(g)+O2(g)==2NO2(g)△H3=-112.30kJ/mol。
若NO2气体和CO气体反应生成无污染气体,其热化学方程式为______________。
(2)某温度下,向10L密闭容器中分别充入0.1molNO2和0.2molCO,发生反应:2NO2(g)+4CO(g)=N2(g)+4CO2(g),经10min反应达到平衡,容器的压强变为原来的![]() 。
。
①0~10min内,CO的平均反应速率v(CO)=__________;
②若容器中观察到_____,可判断该反应达到平衡状态;
③为增大污染物处理效率,起始最佳投料比为______;
④平衡后,仅将CO、CO2气体浓度分别增加一倍,则平衡_____(填“右移”或“左移”或“不移动”)。

(3)在高效催化剂作用下用NH3还原NO2进行污染物处理。
①相同条件下,选用A、B、C三种催化剂进行反应,生成氮气的物质的量与时间变化如图a。活化能最小的是______(用E(A)、E(B)、E(C)表示三种催化剂下该反应活化能)。
②在催化剂A作用下测得相同时间处理NO2的量与温度关系如图b。试说明图中曲线先增大后减小的原因________(假设该温度范围内催化效率相同)。

(4)有人设想在含有NO2的酸性污水中加人填充有铝粉的多孔活性炭颗粒进行水的净化。试结合电极反应说明多孔活性炭的主要作用_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com