
| A. | 焓变是指1mol物质完全参加反应时的能量变化 | |
| B. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| C. | 已知:2HI(g)?H2(g)+I2(g)△H=8.8kJ•mol-1,若向密闭容器中充入1molHI(g),则分解过程中吸收的热量为4.4kJ | |
| D. | 对于反应3H2(g)+N2(g)?2NH3(g),若使用催化剂,v正、v逆同等程度加快 |
分析 A、焓变是反应物和生成物的能量差;
B、中和滴定实验时,用待测液润洗锥形瓶会增大待测溶液的体积,多消耗标准液,引起实验误差;
C、根据可逆反应不可能反应到底分析;
D、使用催化剂同等程度的改变反应速率.
解答 解:A、焓变是反应物和生成物的能量差,不一定是1mol物质反应,故A错误;
B、中和滴定实验时,用待测液润洗锥形瓶会增大待测溶液的体积,多消耗标准液,引起实验误差;依据误差分析判断测得结果增大,故B错误;
C、因为可逆反应不可能反应到底,所以向密闭容器中充入1molHI(g),则分解过程中吸收的热量小于4.4kJ,故C错误;
D、因为催化剂同等程度的改变反应速率,所以使用催化剂,v正、v逆同等程度加快,故D正确;
故选D.
点评 本题比较基础,主要考查△H的含义,中和滴定实验,可逆反应的特征以及催化剂对反应速率的影响,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸与氢氧化钡反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2 H2O | |
| B. | 碳酸钙与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O | |
| C. | CO2通入过量的澄清石灰水中 CO2+Ca2++2OH-=CaCO3↓+H2O | |
| D. | 钠投入硫酸铜溶液中:2Na+Cu2+=2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 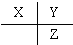 | B. | 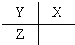 | C. | 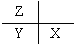 | D. | 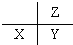 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液除去乙烷中的乙烯 | |
| B. | 用苯与浓溴水在FeBr3催化作用下制溴苯 | |
| C. | 用食醋浸泡有水垢的水壶清除其中的水垢 | |
| D. | 用乙醇从碘水中萃取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 N2H+5+OH-.
N2H+5+OH-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只用溴水一种试剂鉴别苯、己烯、乙醇、四氯化碳 | |
| B. | 用银氨溶液或NaHCO3溶液鉴别甲酸甲酯和乙酸两种液体 | |
| C. | 用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、H+、HCO3-、Cl- | B. | Fe3+、K+、CO32-、NO3- | ||
| C. | K+、Al3+、Cl-、OH- | D. | K+、Ba2+、NO3-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com