
核磁共振氢谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振氢谱图中坐标的位置(化学位移,符号为δ)也就不同。现有一物质的核磁共振氢谱如下图所示,则它可能是

A.CH3CH2CH3 B.CH3CH2CH2OH C.(CH3)2CHCH3 D.CH3CH2CHO
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源:2014-2015学年天津市宝坻区四校高一11月联考化学试卷(解析版) 题型:选择题
A2、B2、C2 3种单质和它们离子间能发生下列反应2A—+C2=2C—+ A2,2C—+ B2 = 2B— + C2,若X—能与C2发生反应2X— + C2 = 2C— + X2 有关说法中不正确的是
A.氧化性B2>C2>A2 B.还原性X->C->B-
C.X2 与B— 能发生反应 D.X2 与B— 不能发生反应、
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市宝坻区四校高二11月联考化学试卷(解析版) 题型:选择题
对于:2C4H10(g)+13O2(g)===8CO2(g)+10H2O(l) ΔH=-5 800 kJ·mol-1的叙述错误的是
A.该反应的反应热为ΔH=-5 800 kJ·mol-1,是放热反应
B.该反应的ΔH与各物质的状态有关,与化学计量数也有关
C.该式的含义为:25 ℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2和液态水时放出热量5800 kJ
D.该反应为丁烷燃烧的热化学方程式,由此可知丁烷的燃烧热为5800 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高二上期期中化学试卷(解析版) 题型:选择题
已知:正四面体形分子E和直线形分子G反应,生成四面体形分子L和直线形分子M(组成E分子的元素的原子序数均小于10,组成G分子的元素为第三周期元素)。
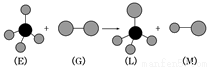
下列判断中正确的是
A.常温常压下,L是一种液态有机物
B.E的二溴代物只有一种结构
C.G具有强氧化性和漂白性
D.上述反应的类型是加成反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高二上期期中化学试卷(解析版) 题型:选择题
A、B两种有机化合物,当混合物总质量一定时,无论A、B以何种比例混合,完全燃烧时产生的CO2的量均相等,肯定符合上述条件的可能是
①同分异构体;②同系物;③具有相同的最简式;④含碳的质量分数相同
A.①③ B.①③④ C.①②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高二上期期中化学试卷(解析版) 题型:选择题
(Ⅰ)1-溴丙烷与2-溴丙烷分别和氢氧化钠的醇溶液混和加热;(Ⅱ)1-溴丙烷与2-溴丙烷分别和氢氧化钠的水溶液混和加热,则下列说法正确的是
A.(Ⅰ)(Ⅱ)产物均相同
B.(Ⅰ)(Ⅱ)产物均不同
C.(Ⅰ)产物相同,(Ⅱ)产物不同
D.(Ⅰ)产物不同,(Ⅱ)产物相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏育才中学高二上学期期中化学试卷(解析版) 题型:实验题
(10分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g。
步骤II:将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数 (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积 (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察 。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂颜色由 色。
(2)滴定结果如下表所示:
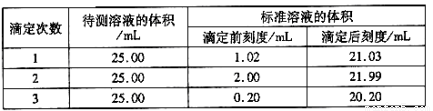
若NaOH标准溶液的浓度为0.1050mol·L-1则该样品中氮的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏育才中学高二上学期期中化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
A.达到化学平衡时,4v正(O2) = 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3) = 3v正(H2O)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏回族自治区银川一中高一上期中化学试卷(解析版) 题型:选择题
下列是某同学对NaHSO4的物质类型进行的分析,其中不正确的是
A.根据元素组成可判断是化合物
B.因它电离会生成钠离子又符合盐的组成,故可属于钠盐
C.因它电离会生成硫酸根离子又符合盐的组成,故可属于硫酸盐
D.NaHSO4溶于水可电离出氢离子故可以称为酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com