
| A. | 当一个可逆反应达到平衡状态时,这个反应的正、逆反应速率相等 | |
| B. | 化学平衡状态是一种静止状态,因为反应物和生成物的浓度已经不再改变 | |
| C. | 当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的最大限度 | |
| D. | 化学反应的限度不可以通过改变条件而改变 |
分析 在不同的条件下,化学反应限度不同,当达到化学反应限度时,正逆反应速率相等但不为0,反应物的浓度和生成物的浓度不再改变,当外界条件发生改变,平衡发生移动,化学反应限度变化.
解答 解:A.在一定条件下,当正逆反应速率相等时,可逆反应达到一定的限度,即平衡状态,故A正确;
B.化学平衡状态是一种动态平衡状态,正逆反应速率相等,对各物质来说消耗与生成的量相等,因为反应物和生成物的浓度不随时间的改变而改变,故B错误;
C.当达到化学反应限度时,反应物的浓度和生成物的浓度不再改变,反应物在该条件下的转化率最大,故C正确;
D.当外界条件发生改变,平衡发生移动,化学反应限度变化,故D错误;
故选AC.
点评 本题考查化学反应平衡状态的判断题目难度不大,本题注意正确理解化学反应限度的特征,易错点为B,注意化学反应平衡状态的本质原因是正逆反应速率相等,浓度不变是外观特征.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 无机物 | B. | 有机物 | C. | 盐类 | D. | 单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水能区分乙酸、乙烯、苯、四氯化碳 | |
| B. | 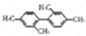 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| C. | 甘氨酸(H3N-CH2COOH)、丙氨酸[CH3CH(NH2)COOH]、谷氨酸[HOOC-CH2CH2CH(NH2)COOH]一定条件下形成链状三肽的结构最多有3种 | |
| D. | 1mol有机物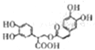 一定条件下能和6molNaOH反应 一定条件下能和6molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiC中硅元素的化合价为-4价,SiC属于共价化合物 | |
| B. | 标准状况下,22.4LCCl4中所含共价键数目为4NA | |
| C. | 该反应中CCl4是还原剂 | |
| D. | 每转移8mol电子,会生成1molSiC |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O.
.亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
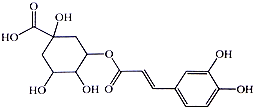 银翘的金银花与连翘配成的中成药,具有辛凉解表,清热解毒,用于流行感冒引起的发热、咳嗽、口干、咽喉肿痛.其中的一种具有较广泛的杀菌作用的有效成分--绿原酸,结构简式见图.下列描述错误的是( )
银翘的金银花与连翘配成的中成药,具有辛凉解表,清热解毒,用于流行感冒引起的发热、咳嗽、口干、咽喉肿痛.其中的一种具有较广泛的杀菌作用的有效成分--绿原酸,结构简式见图.下列描述错误的是( )| A. | 绿原酸有可能通过酯化反应人工合成 | |
| B. | 1mol绿原酸能与4molBr2发生加成反应 | |
| C. | 1mol绿原酸能与6molNa发生置换反应 | |
| D. | 绿原酸能与NaHCO3溶液发生反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 8:7 | B. | 2:7 | C. | 1:1 | D. | 1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com