
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
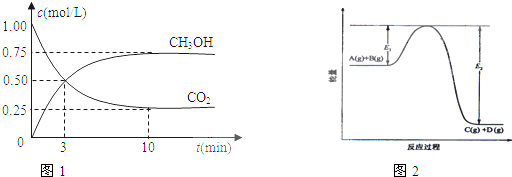
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
(1)如果反应物的总能量大于生成物的总能量,那么该反应是_________反应,举出三个此类反应,要求能用离子方程式表示:
①_____________________________;
②_____________________________;
③_____________________________.
(2)如果反应物的总能量小于生成物的总能量,那么该反应是________反应,举出三个此类反应,要求用化学方程式表示:
①_____________________________;
②_____________________________;
③_____________________________.
此类反应发生通常需要___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
①__________________________________________________;
②__________________________________________________;
③__________________________________________________。
(2)再列举三个吸热反应的例子,用化学方程式表示:
①__________________________________________________;
②__________________________________________________;
③__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com