
(12分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶 液。
肼—空气燃料电池放电时:正极的电极反应式是 。
负极的电极反应式是 。
(3)下图是一个电化学过程示意图。
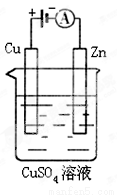
①锌片上发生的电极反应是 。
②假设使用肼 空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼 空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方
程式是 。
(12分,每空2分)
(1)N2H4(1)+O2(g) N2(g)+2H2O(l) △H=-624.0kJ/mol
(2)O2 +4e-+2H2O 4OH- N2H4+4OH--4e-=4H2O+N2↑
(3)①Cu2++2 e- Cu ②112
(4)ClO-+2NH3 N2H4+Cl-+H2O
【解析】
试题分析:(1)32.0gN2H4的物质的量是1mol,所以1molN2H4完全燃烧生成氮气和液态水放出的热量是624kJ,则N2H4完全燃烧反应的热化学方程式是N2H4(1)+O2(g) N2(g)+2H2O(l) △H=-624.0kJ/mol;
(2)燃料电池中正极发生还原反应,元素的化合价降低,所以是氧气发生还原反应,结合电解质溶液,正极反应的电极反应式为O2 +4e-+2H2O 4OH-,负极则是燃料发生反应,根据(1)判断N2H4的氧化产物是氮气,所以负极反应式为N2H4+4OH--4e-=4H2O+N2↑;
(3)①该装置是电解池装置,Zn是阴极,发生还原反应,所以是铜离子得电子发生还原反应,电极反应式为Cu2++2 e- Cu;
②铜片作阳极,发生氧化反应,所以Cu片逐渐溶解,质量减少128g,即Cu的物质的量减少2mol,失去电子4mol,根据整个过程满足得失电子守恒规律,所以氧气得电子的物质的量也是4mol,根据O2 +4e-+2H2O 4OH-,得需要氧气得物质的量是1mol,标准状况下的体积是22.4L,空气中氧气体积含量为20%,所以需要空气的体积是22.4L/20%=112L;
(4)NaClO氧化NH3,制得肼的稀溶液,则Cl元素被还原为氯离子,根据元素守恒,产物中还有水生成,离子方程式为ClO-+2NH3 N2H4+Cl-+H2O。
考点:考查热化学方程式的书写,电化学理论的应用


科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)1.3原子结构 题型:选择题
钠原子变成钠离子的过程中发生变化的是 ( )
A.电子层数 B.质量数
C.质子数 D.中子数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:选择题
在密闭容器中进行反应X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Z为0.2 mol·L-1 B.Y2为0.35 mol·L-1
C.X2为0.3 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(B类)试卷(解析版) 题型:选择题
对于可逆反应:2A(g)+B(g)  2C(g) △H<0,下列图象正确的是( )
2C(g) △H<0,下列图象正确的是( )
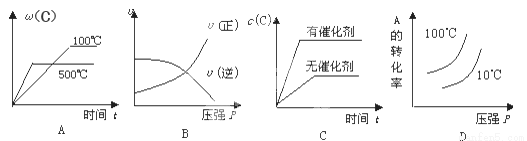
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(B类)试卷(解析版) 题型:选择题
下列有关说法正确的是
A.放热反应在任何条件都能自发进行
B.应用盖斯定律,可计算某些难以直接测量的反应焓变
C.任何能使熵值增大的过程都能自发进行
D.△H>0,△S<0的化学反应一定能自发进行
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(A类)试卷(解析版) 题型:选择题
已知25℃,Fe(OH)3(s)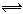 Fe3+(aq)+3OH-(aq),Ksp;Fe3+(aq)+3H2O(l)
Fe3+(aq)+3OH-(aq),Ksp;Fe3+(aq)+3H2O(l)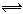 Fe(OH)3(s)+3H+(aq),Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是( )
Fe(OH)3(s)+3H+(aq),Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是( )
A.Kh/Kw=Ksp B.Ksp·Kw=Kh
C. Ksp·Kh=(Kw)3 D.Kw/Kh=(Ksp)3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(A类)试卷(解析版) 题型:选择题
对于可逆反应:2A(g)+B(g) 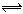 2C(g) △H<0,下列图象正确的是( )
2C(g) △H<0,下列图象正确的是( )
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏江阴高一上暑期学习反馈(开学检测)化学试卷(解析版) 题型:选择题
对于等质量的SO2和SO3来说,下列关系中正确的是
A.含氧原子的个数比为2:3 B.含硫元素的质量比为5:4
C.含氧元素的质量比为6:5 D.含硫原子的个数比为1:1
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:填空题
:如图所示,在一定温度下,把2体积N2和6体积H2通入一个带有活塞的容积可变的容器中,活塞的一端与大气相通,容器中发生以下反应: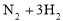

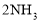 (正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题:
(正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题:

(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:
①若a=1,c=2,则b=_________。在此情况下,反应起始时将向_________(填“正”或“逆”)反应方向进行。
②若需规定起始时反应向逆反应方向进行,则c的取值范围是_________。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是_________,原因是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com