
【题目】石墨烯(图 a)是一种由单层碳原子构成的平面结构新型导电材料,具有大п共轭体系。石墨烯 中部分碳原子被氧化后,其平面结构发生改变,转化为氧化石墨烯(图b)。
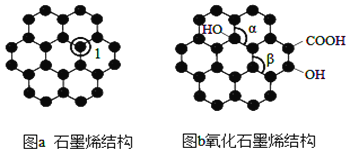
(1)图a中,1号C的杂化方式为______,石墨烯中含有的化学键类型是_____(填极性键,非极性键);图b中键角α____键角β(填“ >”、“<”或“=”),水分子的空间构型是____。
(2)基态钒原子的价电子排布式为______。
(3)醋酸铜可合成复合材料石墨烯![]() ,其制备原料为CuSO4、NH3·H2O和醋酸等。
,其制备原料为CuSO4、NH3·H2O和醋酸等。
①写出一种与SO42-互为等电子体的分子______。
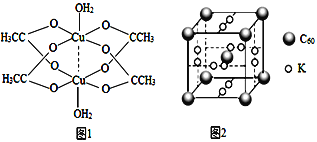
②二聚醋酸铜的结构示意图如图1所示,Cu2+的配位数为______。
(4)石墨烯可转化为富勒烯(C60),C60和K能形成新型化合物,其晶胞如图2所示,晶胞边长参数为anm,该化合物中K原子和C60分子的个数比为_____,该晶体的密度ρ=_____ g.cm-3
【答案】sp2 非极性键 < V形 3d34s2 CCl4 5 3:1 ![]()
【解析】
根据图示原子间的成键方式分析原子的轨道杂化类型及共价键的极性;根据核外电子排布规律书写相关原子的电子排布式;根据等电子体原理及价层电子对互斥模型分析分子的空间构型及判断等电子体;根据配合物的组成及原理分析中心原子的配位数;根据晶胞结构计算晶胞密度。
(1)图a中,与1号C相连的C原子数为3,所以1号C与相邻C形成3个σ键,杂化方式为sp2;石墨烯中含有的化学键为非极性共价键;β角的中心碳是处在平面六边形中的,键角为120°,α角的中心碳周围连了4个单键,与甲烷的结构类似,键角小于120°,所以图b中键角α<键角β;水分子中氧原子轨道杂化类型为sp3,与H原子形成2个σ键,有两对孤电子对,所以分子空间构型为V形.
(2)V的原子序数为23,根据核外电子排布规律分析知基态钒原子的电子排布式为1s22s22p63s23p63d34s2,则价电子排布式为3d34s2。
(3)①等电子体是指价电子总数和原子总数相同的分子、离子或基团,SO42-共有32个价电子,5个原子,用“替代法”,CCl4或SiCl4中的价电子总数均为4+4×7=32,且都有5个原子,所以与SO42-互为等电子体。
②由图可知二聚醋酸铜中,有2个铜离子、2个水分子、4个醋酸根离子,则其化学式为Cu2(CH3COO)4(H2O)2,根据图示,Cu2+的配位数为5。
(4)如图所示,有12个K原子位于面上,则一个晶胞中K原子数为12×1/2=6,有8个C60位于顶点处、1个C60位于体心,则一个晶胞中C60分子数为8×1/8+1=2,该化合物中K原子和C60分子的个数比为6:2=3:1,一个晶胞的质量为![]() ,则该晶体的密度ρ=
,则该晶体的密度ρ=![]() g÷(a×10-7cm)3=
g÷(a×10-7cm)3=![]() g/cm3。
g/cm3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】两种金属混合物共15g,投入足量的盐酸中,充分反应后得到11.2LH2(标准状况),则原混合物的组成肯定不可能为( )
A. Mg和AlB. Zn和MgC. Al和ZnD. Al和Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A是生石灰的主要成分,B是一种具有漂白性的无色气体,D是一种常见的无色液体,F是某种补血剂的有效成分,G是一种常见的强酸,H的摩尔质量为72 g·mol-1。

(1)A的化学式为____________。
(2)D的电子式为____________。
(3)写出反应①的化学方程式:________________________。
(4)写出反应②的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象及结论均正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 黄色溶液中只含Br2 |
B | 烧杯中看见白色沉淀 | 证明酸性强弱:H2CO3>H2SiO3 |
C | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液;未出现银镜 | 蔗糖未水解 |
D | pH试纸先变红后褪色 | 氯水既有酸性,又有漂白性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】头孢拉定又名先锋霉素,是常用的一种抗生素,其结构简式如下:
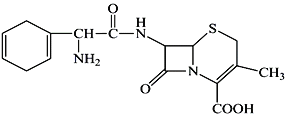
下列说法不正确的是 ( )
A. 头孢拉定的分子式是C16H19N3O4S,分子中有多种官能团
B. 头孢拉定与Na2CO3溶液、NaHCO3溶液都可以反应
C. 头孢拉定既可与盐酸反应,也可与NaOH溶液反应
D. 1mol头孢拉定最多可与5mol H2和3mol Br2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国药物学家最近合成一种可能用于治疗高血压的有机物K,合成路线如下:
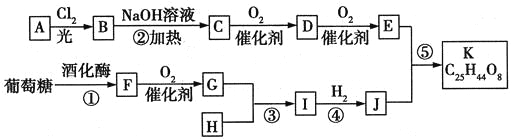
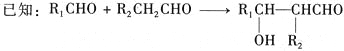
其中A属于碳氢化合物,其中碳的质量分数约为83.3%;E的核磁共振氢谱中只有2组吸收峰。H常温下呈气态,是室内装潢产生的主要污染物之一。G和H以1:3反应生成I。
试回答下列问题:
(1)A的分子式为:______________。
(2)写出下列物质的结构简式:D:____________;G:___________。
(3)反应①―⑤中属于取代反应的有___________。
(4)反应①的化学方程式为_______________;反应④的化学方程式为_________________。
(5)E有多种同分异构体,符合“既能发生银镜反应又能发生水解反应”条件的E的同分异构体有_______种,写出符合上述条件且核磁共振氢谱只有2组吸收峰的E的同分异构体的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如图:
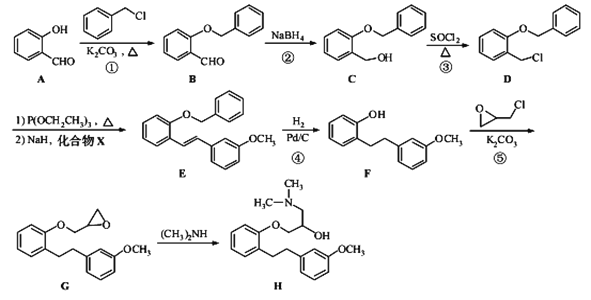
(1)化合物A中的含氧官能团为___和___(填官能团名称)。
(2)反应⑤的反应类型是___,反应方程式___。
(3)B的分子式___,1molB与足量的银氨溶液反应,最多能产生___gAg。
(4)检验D中卤原子种类,所需的试剂有___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
a.分子中含有两个苯环;
b.分子中有7种不同化学环境的氢;
c.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花椒毒素(Ⅰ)是白芷等中草药的药效成分,也可用多酚A为原料制备,合成路线如下:

回答下列问题:
(1)①的反应类型为_____________________;B分子中最多有_________个原子共平面。
(2)C中含氧官能团的名称为______________________;③的“条件a”为____________________。
(3)④为加成反应,化学方程式为__________________________________。
(4)⑤的化学方程式为__________________________________。
(5)芳香化合物J是D的同分异构体,符合下列条件的J的结构共有_________种,其中核磁共振氢谱为五组峰的J的结构简式为_________________。(只写一种即可)。
①苯环上只有3个取代基;②可与NaHCO3反应放出CO2;③1mol J可中和3mol NaOH。
(6)参照题图信息,写出以 为原料制备
为原料制备 的合成路线(无机试剂任选) :______________
的合成路线(无机试剂任选) :______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com