
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)吸收液吸收SO2的过程中,pH随n(SO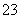 )∶n(HSO
)∶n(HSO )变化关系如下表:
)变化关系如下表:
| n(SO | 91∶9 | 1∶1 | 9∶91 |
| pH | 8.2 | 7.2 | 6.2 |
由上表判断,NaHSO3溶液显________性,用化学平衡原理解释:________________________________________________________________________。
(2)当吸收液的pH降至约为6时,需送到电解槽再生。再生示意图如下:
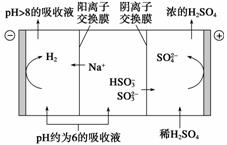
当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
________________________________________________________________________。
科目:高中化学 来源: 题型:
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g) 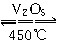 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可制备出超高强度的高性能混凝土。下列关于二氧化硅的说法中,正确的是
( )
A.二氧化硅溶于水生成硅酸,所以二氧化硅属于酸性氧化物
B.将二氧化碳通入硅酸钠溶液中可以得到硅酸
C.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强
D.水晶是比较纯净的二氧化硅,沙子的主要成分是硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表述正确的是________(填序号)。
①(四川理综,4D)将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色
②(天津理综,3B)NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
③(重庆理综,3D)25 ℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
④(安徽理综,12D)溶解度小的沉淀易向溶解度更小的沉淀转化,ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀
⑤(江苏,11C)加热0.1 mol·L-1 Na2CO3溶液,CO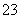 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大
⑥(北京理综,9A)测0.1 mol·L-1氨水的pH为11:NH3·H2ONH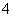 +OH-
+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO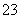 水解
水解
C.将饱和FeCl3溶液滴入沸水中可制备Fe(OH)3胶体,利用的是盐类水解原理
D.纯碱溶液呈碱性的原因是:CO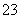 +H2OHCO
+H2OHCO +OH-
+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化曲线如下图所示。下列说法错误的是( )
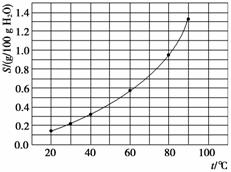
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH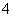 )=c(Cl-),则溶液显__________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=______________________________________________________。
)=c(Cl-),则溶液显__________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
20 ℃时向20 mL 0.1 mol·L-1醋酸溶液中不断滴入0.1 mol·L-1 NaOH溶液,溶液pH变化如图所示。此过程中离子浓度的关系错误的是( )
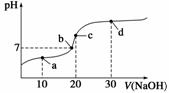
A.a点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.b点:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
C.c点:c(H+)=c(CH3COOH)+c(OH-)
D.d点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

(1)由图中信息可知HA为________酸(填“强”或“弱”),理由是
__________________________________________________________。
(2)常温下一定浓度的MA稀溶液的pH=a,则a________7(填“>”、“<”或“=”),用离子方程式表示其原因:________________,此时,溶液中由水电离出的c(OH-)=____________。
(3)请写出K点所对应的溶液中离子浓度的大小关系:________________________________。
(4)K点对应的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”、“<”或“=”);若此时溶液的pH=10,则c(MOH)+c(OH-)≈________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com