
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.l mol·L-1CuSO4·(NH4)2SO4·6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-)
C.0.1 mol·L-1NaHCO3溶液中: c(Na+)+c(H+) =c(HCO3-)+2c(CO32-)+c(OH-)
D.等V、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)
科目:高中化学 来源:2016届湖北省高三9月调考化学试卷(解析版) 题型:选择题
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:

已知转化过程中的反应为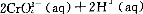
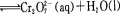
转化后所得溶液中铬元素的含量为28.6 g/L, CrO42-有10/11转化为Cr2072-,下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到平衡状态
B.若用绿矾(FeS04·7H2O)作还原剂,处理1 L废水,至少需要458.7g
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5
D.常温下Ksp=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
在密闭容器中发生可逆反应4NH3+5O2 4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
A.v(O2)=0.001mol/(L·S)
B.v(NH3)=0.002 mol/(L·S)
C.v(H2O)=0.003 mol/(L·h)
D.v(NO)=0.008 mol/(L·S)
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三上12月联考理综化学试卷(解析版) 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某小组模拟制备氨基甲酸铵的反应为:2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
(1)如用下图装置和选用的试剂制取氨气,其中错误的是________;氨气的实验室制法的化学方程式是 。
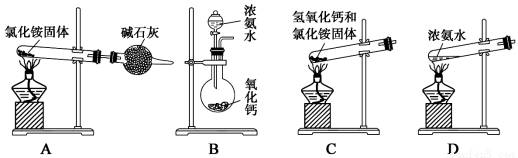
(2)制备氨基甲酸铵的装置如下图所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中。 当悬浮物较多时,停止制备。(注:CCl4与液体石蜡均为惰性介质。)
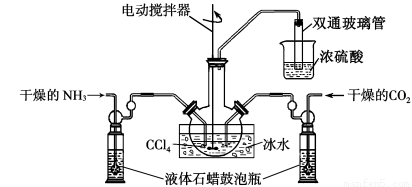
①发生器用冰水冷却的原因是 ;
液体石蜡鼓泡瓶的作用是 ;
双通玻璃管的作用是 ;
浓硫酸的作用是 。
②从反应后的混合物中分离出产品的实验方法是 (填写操作名称)。
为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。请利用下列试剂,设计实验方案,对制得的氨基甲酸铵中的杂质进行成分探究。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:填空题
(Ⅰ)某温度下,NaCl溶液中的c(H+)=2.0×10-7 mol/L,则此时在溶液中:
(1)由水电离产生的c(OH-)= ;
(2)若温度不变,滴入稀硫酸使c(H+)=5.0×10-6 mol/L,则c(OH-)= 。
(Ⅱ)(3)某温度下水的离子积为KW =1×10-13,则该温度(填“大于”、“等于”或“小于”)
25℃。
若将此温度下pH=11的NaOH溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过填写以下不同情况时两种溶液的体积比:
(4)若所得混合液为中性,则a∶b= ;
(5)若所得混合液的pH=2,则a∶b= ;
(6)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,若测定结果偏高,其原因可能是 。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH: c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—)>c(CO32—)>c(H2CO3)
C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH+4)>c(OH-)=c(H+)
D.0.2mol·L-1CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c (CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
在BaSO4饱和溶液中加入少量的BaCl2溶液,产生BaSO4沉淀,若以Ksp表 示BaSO4的溶度积常数,则平衡后溶液中
示BaSO4的溶度积常数,则平衡后溶液中
A.c(Ba2+)=c(SO42-)=(Ksp)1/2
B.c(Ba2+)·c(SO42-)>Ksp,c(Ba2+)=c(SO42-)
C.c(Ba2+)·c(SO42-)=Ksp,c(Ba2+)>c(SO42-)
D.c(Ba2+)·c(SO42-)≠Ksp,c(Ba2+)<c(SO42-)
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
室温下,0.1 mol/L的某二元酸H2A溶液中,溶液中可能存在的含A粒子(H2A、HA一、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是
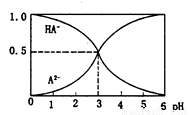
A.H2A的电离方程式:H2A  H十+HA-
H十+HA-
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=l:100
C.等物质的量浓度NaHA和Na2A溶液等体积混合,离子浓度大小关系为:[c(Na+))c(HA-)>c(A2-)
D.Na2A溶液必存在c(OH一)=c(H+)+c(HA-)十2c(H2A),各粒子浓度均大0
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列实验装置设计正确、且能达到目的的是
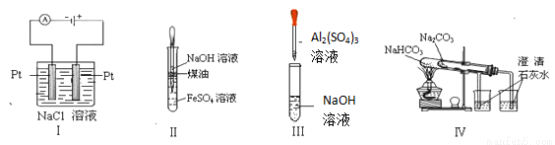
A.实验Ⅰ:制取金属钠
B.实验II:制取Fe(OH)2
C.实验Ⅲ:制取少量的氢氧化铝
D.实验Ⅳ:比较两种物质的热稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com