
| A£® | Ō»ģŗĻĪļÖŠŗ¬ŃõŌ×ÓµÄÖŹĮæĪŖ1.6g | |
| B£® | ŌĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ2.0mol/L | |
| C£® | ·“Ó¦ÖŠ²śÉś±źæöĻĀNOµÄĢå»żĪŖ4.48L | |
| D£® | ¹ĢĢåĪļÖŹČܽāŗóŹ£ÓąHNO3ĪŖ0.2mol |
·ÖĪö ŌŚĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗŗ󣬓ĖŹ±ČÜŅŗ³ŹÖŠŠŌ£¬½šŹōĄė×ÓŅŃĶźČ«³Įµķ£¬ČÜŅŗÖŠČÜÖŹĪŖNaNO3£¬n£ØNaNO3£©=n£ØNaOH£©=1.0mol/L”Į1.0L=1mol£¬¾Ļ“µÓ”¢øÉŌļ”¢×ĘÉÕ£¬µĆµ½ŗŚÉ«¹ĢĢåÖŹĮæĪŖ32gŹĒŃõ»ÆĶµÄÖŹĮ棬ĪļÖŹµÄĮæĪŖ$\frac{32g}{80g/mol}$=0.4mol£¬øł¾ŻĶŌŖĖŲŹŲŗćÓŠn£ØCu£©+2n£ØCu2O£©=n£ØCuO£©£¬ĖłŅŌ·“Ó¦ŗóµÄČÜŅŗÖŠn[[Cu£ØNO3£©2]=n£ØCuO£©=0.4mol£®
A£®ĮīCuŗĶCu2OµÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬øł¾Ż¶žÕßÖŹĮæ¼°CuŌŖĖŲĪļÖŹµÄĮæĮŠ·½³Ģ¼ĘĖć£¬Ō»ģŗĻĪļÖŠŗ¬ŃõŌ×ÓµÄÖŹĮ棻
B£®øł¾ŻNŌŖĖŲŹŲŗćæÉÖŖŌĻõĖįČÜŅŗn£ØHNO3£©=n£ØNO£©+n£ØNaNO3£©£¬øł¾ŻNaŌŖĖŲæÉÖŖn£ØNaNO3£©=n£ØNaOH£©£¬ŌŁøł¾Żc=$\frac{n}{V}$¼ĘĖć£»
C£®ĮīCuŗĶCu2OµÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬øł¾Ż¶žÕßÖŹĮæ¼°CuŌŖĖŲĪļÖŹµÄĮæĮŠ·½³Ģ¼ĘĖć£¬ĄūÓƵē×Ó×ŖŅĘŹŲŗć¼ĘĖćn£ØNO£©£¬ŌŁøł¾ŻV=nVm¼ĘĖćNOµÄĢå»ż£»
D£®øł¾ŻNŌŖĖŲŹŲŗć£¬æÉÖŖnŹ£Óą£ØHNO3£©+2n[[Cu£ØNO3£©2]=n£ØNaNO3£©£¬øł¾ŻNaŌŖĖŲæÉÖŖn£ØNaNO3£©=n£ØNaOH£©£®
½ā“š ½ā£ŗŌŚĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗŗ󣬓ĖŹ±ČÜŅŗ³ŹÖŠŠŌ£¬½šŹōĄė×ÓŅŃĶźČ«³Įµķ£¬ČÜŅŗÖŠČÜÖŹĪŖNaNO3£¬n£ØNaNO3£©=n£ØNaOH£©=1.0mol/L”Į1.0L=1mol£¬¾Ļ“µÓ”¢øÉŌļ”¢×ĘÉÕ£¬µĆµ½ŗŚÉ«¹ĢĢåÖŹĮæĪŖ32gŹĒŃõ»ÆĶµÄÖŹĮ棬ĪļÖŹµÄĮæĪŖ$\frac{32g}{80g/mol}$=0.4mol£¬øł¾ŻĶŌŖĖŲŹŲŗćÓŠn£ØCu£©+2n£ØCu2O£©=n£ØCuO£©£¬ĖłŅŌ·“Ó¦ŗóµÄČÜŅŗÖŠn[[Cu£ØNO3£©2]=n£ØCuO£©=0.4mol£®
ÉčCuŗĶCu2OµÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬øł¾Ż¶žÕßÖŹĮæÓŠ 64x+144y=27.2£¬øł¾ŻĶŌŖĖŲŹŲŗćÓŠx+2y=0.4£¬ĮŖĮ¢·½³Ģ½āµĆx=0.2£¬y=0.1£¬
A£®ŅņĪŖŃõ»ÆŃĒĶµÄÖŹĮæĪŖ0.1mol£¬ĖłŅŌ»ģŗĻĢåĻµÖŠŃõŌ×ÓµÄÖŹĮæĪŖ1.6g£¬¹ŹAÕżČ·£»
B£®øł¾ŻNŌŖĖŲŹŲŗćæÉÖŖn£ØHNO3£©=n£ØNO£©+n£ØNaNO3£©=0.2mol+1.0mol/L”Į1.0L=1.2mol£¬ĖłŅŌŌĻõĖįČÜŅŗµÄÅضČĪŖ$\frac{1.2mol}{0.5L}$=2.4mol/L£¬¹ŹB“ķĪó£»
C£®øł¾Żµē×Ó×ŖŅĘŹŲŗćæÉÖŖ£ŗ3n£ØNO£©=2n£ØCu£©+2n£ØCu2O£©£¬ĖłŅŌ3n£ØNO£©=2”Į0.2mol+2”Į0.1mol£¬½āµĆn£ØNO£©=0.2mol£¬ĖłŅŌČē¹ūŌŚ±ź×¼×“æöĻĀNOµÄĢå»żĪŖ0.2mol”Į22.4L/mol=4.48L£¬¹ŹCÕżČ·£»
D£®·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬ĒāŃõ»ÆÄĘÓėĻõĖįĶ·“Ó¦£¬Ź£ÓąµÄĒāŃõ»ÆÄĘÓėĻõĖį·“Ó¦£¬×īŗóĪŖĻõĖįÄĘČÜŅŗ£¬øł¾ŻµŖŌŖĖŲŹŲŗćæÉÖŖ·“Ó¦ŗóČÜŅŗÖŠn£ØHNO3£©+2n[[Cu£ØNO3£©2]=n£ØNaNO3£©£¬ĖłŅŌn£ØHNO3£©=n£ØNaNO3£©-2n[[Cu£ØNO3£©2]=1mol-2”Į0.4mol=0.2mol£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĶ¼°Ęä»ÆŗĻĪļÖŖŹ¶”¢Ńõ»Æ»¹Ō·“Ó¦µÄ¼ĘĖć£¬ÄŃ¶Č½Ļ“ó£¬Ē峞·“Ó¦¹ż³Ģ£¬³ä·ÖĄūÓĆŹŲŗć¼ĘĖćŹĒ½āĢāµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{{20M”Į{{10}^{-3}}}}{127}$g | B£® | 20M g | C£® | $\frac{{20”Į{{10}^{-3}}}}{M}$g | D£® | $\frac{20}{M}$g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C | B£® | O | C£® | P | D£® | S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶĘ¹ćŹ¹ÓĆĪŽĮ×Ļ“ŅĀ·Ū£¬ŅŌ¼õÉŁĖ®Ģåø»ÓŖŃų»Æ | |
| B£® | PM2.5ŹĒÖø“óĘųÖŠÖ±¾¶½Ó½üÓŚ2.5¦Ģm£Ø1m=106¦Ģm=109nm£©µÄæÅĮ£Īļ£¬Ņ²³ĘæÉĪüČėæÅĮ£Īļ£¬ÕāŠ©ĻøæÅĮ£Īļ·ÖÉ¢ŌŚæÕĘųÖŠŠĪ³ÉµÄ·ÖÉ¢ĻµŹĒ½ŗĢå | |
| C£® | ĪŖĢįøßÅ©×÷Īļ²śĮæ“óĮæŹ¹ÓĆÅ©Ņ©ŗĶ»Æ·Ź | |
| D£® | ¶ŌÅ©×÷Īļ½ÕøŃ½ųŠŠ·ŁÉÕ»¹Ģļ£¬ŅŌŌö¼ÓĶĮČĄ·ŹĮ¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė³-2-¶”Ļ©Óė·“-2-¶”Ļ©ÓėĒāĘų¼Ó³ÉµÄ²śĪļ²»ĻąĶ¬ | |
| B£® | ŠĀĪģĶéµÄ¶žĀČ“śĪļÓŠ2ÖÖ | |
| C£® | ·Ö×ÓŹ½ĪŖC2H4ŗĶC4H8µÄĪļÖŹŅ»¶Ø»„ĪŖĶ¬ĻµĪļ | |
| D£® | ¼üĻߏ½ĪŖ 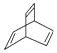 µÄÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC8H10 µÄÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC8H10 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6.02”Į1023 | B£® | 1.204”Į1024 | C£® | 2 | D£® | 1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 15NÖŠŗ¬ÓŠ7øöÖŠ×Ó | |
| B£® | N2ŗĶN70ŹōÓŚĶ¬Ī»ĖŲ | |
| C£® | N5+ÖŠŗ¬ÓŠ36øöµē×Ó | |
| D£® | ČōNH5ĪŖĄė×Ó»ÆŗĻĪļ£¬ŌņĘä¼Čŗ¬ÓŠĄė×Ó¼ü£¬ÓÖŗ¬ÓŠ¹²¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CH2 | B£® | ŅŅ“¼µÄ·Ö×ÓŹ½£ŗCH3CH2OH | ||
| C£® | ¼×ĶéµÄ½į¹¹Ź½£ŗCH4 | D£® | ¼×±½µÄ¼üĻߏ½£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com