
【题目】下列叙述正确的是
A. 含金属元素的离子一定是阳离子
B. 金属阳离子被还原一定得到金属单质
C. 共价化合物中只含共价键
D. 1H、2H、3H互为同素异形体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:Na>MgO>SiO2
B.水溶性:SO2>H2S>HCl
C.热稳定性:HF>H2O>NH3
D.沸点:HF>HCl>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是常见的氧化剂、催化剂和活性电极材料。
(1)工业上,以惰性材料为电极,电解MaSO4溶液(含少量稀硫酸)制备MnO2。写出阳极的电极反应式:_________________________________。
(2)已知如下热化学方程式(K代表平衡常数):
①MnCO3(s)![]() Mn0(s)+CO2(g)△H1 K1
Mn0(s)+CO2(g)△H1 K1
②2MnO(s)+O2(g)![]() 2MnO2(s)△H2 K2
2MnO2(s)△H2 K2
③2MnCO3(n)+O2(g)![]() 2MnO2(s)+2CO2(g)△H3 K3
2MnO2(s)+2CO2(g)△H3 K3
△H3=________用△H1,△H2表示);K3=________用K1、K2表示)。
(3)反应②在低温条件下能自发进行,则△H3________0(填“>"“<"或“=")。
(4)在密闭容器中投入足量的MnCO3,一定条件下发生反应MnCO3(s)![]() MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
MnO(s)+CO2(g) △H>0。在一定湿度下,达到平衡状态时ρ(CO2)=2aMPa。
①温度、压强对MnCO3分解率的影响如图所示:
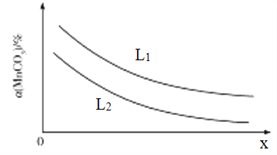
比较:L1__________L2(填“>"“<”或“=")。
②保持温度不变,将容器休积扩大至原来的2倍,则ρ(CO2)的变化范围是____________。
③保持温度不变,将容器体积压缩至原来的一半,达到新平衡时下列物理量一定不变的是____(填代号)。
A.平衡常数K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)一定温度下,在容积为2L的恒容密闭容器中加入足量的MnCO3(s)和5molO2,发生反应:2MnCO3(s)+O2(g)![]() 2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
2MnO2(s)+2CO2(g),CO2以平均速率为0.1mol·L-1·min-1经过10min达到平衡状态,该条件下该反应的平衡常数K为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境保护是当今倍受人们关注的社会问题.下列叙述不正确的是( )
A.二氧化硫会形成酸雨
B.氮氧化物会形成光化学烟雾
C.过度使用煤作能源会引起雾霾等环境危害
D.一氧化碳是造成温室效应的主要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学和环境保护、食品营养、材料应用等密切相关.
(1)防治环境污染、改善生态环境已成为全人类的共识.
①下列各项中,完成空气质量报告时不需要监测的是 (填字母).
a.二氧化碳的浓度 b.二氧化硫的浓度 c.可吸入颗粒物的浓度
②煤的气化是是高效、清洁地利用煤炭的重要途径,写出制备水煤气的化学方程式 ;
③下列做法中不利于改善环境质量的是 (填字母).
a.将废旧电池进行深埋处理
b.充分利用风能等新能源
c.给汽车加装尾气催化净化装置
④工业废水需处理达标后才能排放.轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是 (填字母).
a.氧化还原法 b.中和法 c.沉淀法
⑤居室环境污染严重危害我们的健康,装修材料挥发出 和 是常见的居室环境污染物;存在于石材中的氡因具有 性,也是常见的居室环境污染物。
(2)营养平衡、合理用药是保证人体健康和生活质量的重要途径.
①在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是 .(填元素符号)
②下列物质中,具有抗菌消炎疗效的是 (填字母).
a.氨基酸 b.阿斯匹林 c.青霉素
③如图为某品牌鸡精标签的一部分,其中能水解生成氨基酸的配料是 ,属于着色剂的是 ,属于防腐剂的是 .

(3)材料是人类社会发展的物质基础,材料科学的发展离不开化学.
①水泥、玻璃及陶瓷都是传统的硅酸盐材料,生产水泥和玻璃都用到的原料是 ; SiC是一种新型的陶瓷,工业上用石英砂与焦炭高温下条件下生成SiC同时生成CO,该制备反应的化学方程式为
②钢铁制品在潮湿的空气中发生 (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因.写出钢铁发生吸氧腐蚀时的正极反应
③橡胶是制造轮胎的重要原料,天然橡胶通过 (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
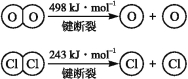
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 需要加热才能发生的反应一定是吸热反应
B. 放热反应在常温下一定很容易发生
C. 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小
D. 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实:
(1)X+Y2+===X2++Y
(2)Z+2H2O![]() Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+离子的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是()
A. X>Y>Z>W B. Y>X>W>Z
C. Z>X>Y>W D. Z>Y>X>W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com