
【题目】利用木质纤维可合成药物中间体H,还能合成高分子化合物G,合成路线如下:
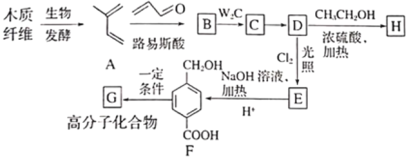
已知:①
②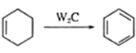
(1)A的化学名称是___________。
(2)B的结构简式是___________,由C生成D的反应类型为___________。
(3)化合物E的官能团为___________。
(4)F分子中处于同一平面的原子最多有___________个。D生成E的化学反应方程式为___________。
(5)芳香化合物I为H的同分异构体,苯环上一氯代物有两种结构,1molI发生水解反应消耗2 mol NaOH,符合要求的同分异构体有___________种,其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6︰3︰2︰1的I的结构简式为___________。
(6)写出用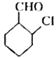 为原料制备
为原料制备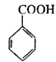 的合成路线(其他试剂任选)___________。
的合成路线(其他试剂任选)___________。
【答案】2-甲基-1,3-丁二烯 ![]() 氧化反应 氯原子、羧基 17
氧化反应 氯原子、羧基 17 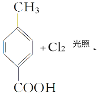
 10
10 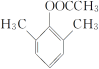 、
、


【解析】
结合框图和各步反应条件分析各物质结构简式为:由 可知,
可知,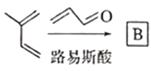 生成的B的结构简式为
生成的B的结构简式为![]() ,再根据
,再根据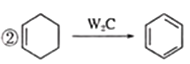 可知C为
可知C为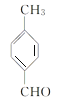 、D为
、D为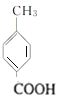 、H为
、H为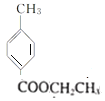 、E为
、E为 、F为
、F为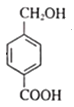 。结合各物质的性质进行解答。
。结合各物质的性质进行解答。
(1)由![]() 结构简式可知A的化学名称是2-甲基-1,3-丁二烯;答案:2-甲基-1,3-丁二烯;
结构简式可知A的化学名称是2-甲基-1,3-丁二烯;答案:2-甲基-1,3-丁二烯;
(2)结合上述分析可知B的结构简式是![]() ,由C为
,由C为 ,D为
,D为 可知,C生成D的反应类型为氧化反应。答案:
可知,C生成D的反应类型为氧化反应。答案:![]() ;氧化反应;
;氧化反应;
(3)结合上述分析可知E为 ,化合物E的官能团为氯原子、羧基;答案:氯原子、羧基。
,化合物E的官能团为氯原子、羧基;答案:氯原子、羧基。
(4)结合上述分析可知F为 ,苯环上12个原子共面,碳氧双键可以共面,单键可以旋转,所以羟基也可以共面,所以F分子中处于同一平面的原子最多有17个。由D为
,苯环上12个原子共面,碳氧双键可以共面,单键可以旋转,所以羟基也可以共面,所以F分子中处于同一平面的原子最多有17个。由D为 ,E为
,E为 可知,D生成E的化学反应方程式为
可知,D生成E的化学反应方程式为
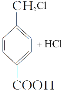 ;答案:.
;答案:. 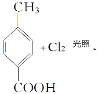
 。
。
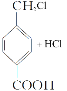
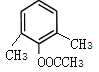
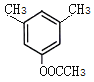
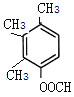
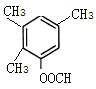
(5) H为 ,芳香化合物I为H的同分异构体,其苯环上一氯代物有两种结构,1molI发生水解反应消耗2 mol NaOH,则I为酚酯。符合要求的同分异构体有
,芳香化合物I为H的同分异构体,其苯环上一氯代物有两种结构,1molI发生水解反应消耗2 mol NaOH,则I为酚酯。符合要求的同分异构体有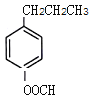 、
、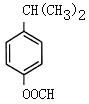 、
、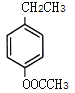 、
、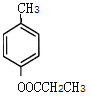 、
、 、
、 、
、 、
、 、
、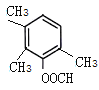 、
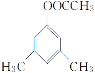
、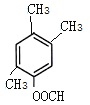 ,共10种,其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6︰3︰2︰1的I的结构简式为
,共10种,其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6︰3︰2︰1的I的结构简式为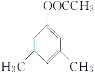 ,
,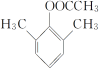 。答案:10,
。答案:10, ,
, .
.
(6)结合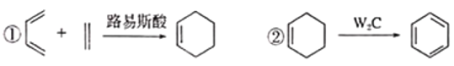 ,用
,用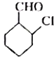 为原料制备
为原料制备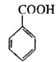 ,先发生消去反应在环上形成双键,然后发生脱氢反应生成苯环,最后发生氧化反应即可。具体的合成路线如下:
,先发生消去反应在环上形成双键,然后发生脱氢反应生成苯环,最后发生氧化反应即可。具体的合成路线如下: 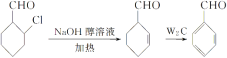
 ;答案:
;答案: 
 。
。


科目:高中化学 来源: 题型:
【题目】下列情况会使所配溶液浓度偏低或其他测量值偏低的是( )
①用稀醋酸和稀氢氧化钠溶液反应测定中和热数值;②用滴定管量取液体时,开始时平视读数,结束时俯视读数所得溶液的体积;③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤;④在用标准液(已知浓度)滴定未知溶液时,盛标准液的滴定管水洗后未润洗;⑤定容时,仰视容量瓶的刻度线
A. ①③⑤B. ①②⑤
C. ②③④D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物VL(标准状况)溶于mg水中,得到溶液的质量分数为ω%,物质的量浓度cmol/L,密度为ρg/cm3,则下列说法正确的是
A. 相对分子质量M可表示为:![]()
B. 溶液密度ρ可表示为:![]()
C. 溶液的质量分数ω%可表示为:![]()
D. 物质的量浓度C可表示为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法合理的是
①根据纯净物中是否含氧元素,来判断是否属于氧化物
②根据电泳现象可证明胶体带电荷
③直径介于lnm~l00nm之间的微粒称为胶体
④金属氧化物都是碱性氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液
⑥同一钢笔使用不同牌号的墨水容易堵塞,是由于胶体的聚沉
A. 只有⑥ B. 只有②⑥ C. 只有③④⑤ D. 只有①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:__Fe2+___ClO-+( )___=____Fe(OH)3↓+__C1﹣+( )。
②检验滤液B中是否还含有铁元素的方法为:________(注明试剂、现象)。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、____(填操作名称)、洗涤。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1LpH=6的纯水中含有OH-的数目为10-8NA
B.当氢氧酸性燃料电池中转移2mol电子时被氧化的分子数为NA
C.0.5mol雄黄(As4S4,结构如图![]() ),含有NA个S—S键
),含有NA个S—S键
D.一定条件下向密闭容器中充入1molH2和2molH2(g)充分反应,生成HI分子数最多等于2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如下图所示,下列有关说法错误的是
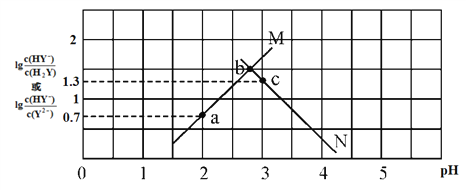
A. 曲线 M 表示 pH与 lg![]() 的变化关系
的变化关系
B. a点溶液中:c(H+) ― c(OH-)=2c(Y2-)+c(HY-) ― c(K+)
C. H2Y 的第二级电离常数Ka2(H2Y)=10-4.3
D. 交点b的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如下:

(1)A分子中含有的官能团的名称是____________________________________。
(2)A、B能否与NaOH溶液反应:A________(填“能”或“不能”,下同),B________。
(3)A在浓硫酸作用下加热可得到B,其反应类型是____________________。
(4)A、B各1 mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是________mol、________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com