
【题目】通过图像分析影响化学平衡移动的因素,某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g) 2SO3(g) ΔH<0的正、逆反应速率的影响如图所示:

①加催化剂对反应速率影响的图像是___(填字母,下同),平衡____移动。
②升高温度对反应速率影响的图像是___,平衡向____方向(填“正反应”或“逆反应”,下同)移动。
③增大反应容器体积对反应速率影响的图像是___,平衡向____方向移动。
④增大O2的浓度对反应速率影响的图像是___,平衡向____方向移动。
⑤上述①到④中的外界条件,使得单位体积内活化分子百分数增大的是___(填序号)。
【答案】C不A逆反应D逆反应B正反应①②
【解析】
①加入催化剂,正逆反应速率同时增大,且增大幅度相同,催化剂不影响化学平衡;
②该反应为放热反应,升高温度,正逆反应速率都增大,由于平衡向着逆向移动,逆反应速率增大幅度大于正反应速率;
③增大反应容器体积,减小了压强,正逆反应速率都减小,平衡向着体积增大的逆反应方向移动;
④增大反应物浓度的瞬间,正反应速率增大,逆反应速率不变,随反应进行正反应速率逐渐减小,逆反应速率逐渐增大,直至达到新的平衡.
⑤升高温度、加入催化剂可增大活化分子的百分数,而增大压强、增大浓度,可增大单位体积活化分子的数目,但百分数不变。
①催化剂只影响反应速率,不影响化学平衡,所以加入催化剂后正逆反应速率同时增大且相等,化学平衡不发生移动,所以C正确;
②升高温度后,正反应速率和逆反应速率都增大,由于该反应为放热反应,平衡向着逆反应方向移动,说明逆反应速率大于正反应速率,所以A正确;
③该反应为体积缩小的反应,增大反应容器体积,反应体系压强减小,正逆反应速率都会减小,平衡向着体积增大的逆反应方向移动,说明逆反应速率减小幅度减小,即逆反应速率大于正反应速率,满足该变化的图象为D;
④增大O2的浓度的瞬间,逆反应速率不变,正反应速率增大,平衡向着正反应方向移动,满足该变化的图象为B.
⑤升高温度、加入催化剂可增大活化分子的百分数,而增大压强、增大浓度,可增大单位体积活化分子的数目,但百分数不变。故选 ①②。


科目:高中化学 来源: 题型:
【题目】(题文)[化学——选修5:有机化学基础]
近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下:
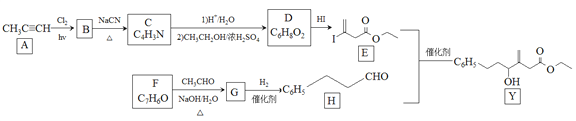
已知:![]()
回答下列问题:
(1)A的化学名称是________________。
(2)B为单氯代烃,由B生成C的化学方程式为________________。
(3)由A生成B、G生成H的反应类型分别是________________、________________。
(4)D的结构简式为________________。
(5)Y中含氧官能团的名称为________________。
(6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。
(7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,其中X原子最外层电子数是内层电子数的两倍,元素Y的核电荷数等于W原子的最外层电子数,Z在空气中燃烧发出耀眼的白光。下列说法正确的是
A. X和Y的氧化物都是可导致酸雨的污染物
B. Z和W形成的化合物中既有离子键又有共价键
C. 最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X
D. 原子半径由大到小的顺序:r(X)>r(Y)>r(Z)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH1
②C(s)+O2(g)===CO2(g) ΔH2
③H2(g)+1/2O2(g)===H2O(l) ΔH3
则反应④2C(s)+H2(g)===C2H2(g)的ΔH=_________。(用含ΔH1、ΔH2、ΔH3的关系式表示)
(2)利用上述反应①设计燃料电池(电解质溶液为氢氧化钾溶液),写出电池的负极反应式:___________。
(3)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/(mol·L-1) 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①1~10 min内,NO的平均反应速率
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的NO
b.加入一定量的C
c.适当升高反应体系的温度
d.加入合适的催化剂
e.适当缩小容器的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4v正(O2)=5v逆(NO)
B. 若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到平衡时,若减小容器体积,则NH3的转化率会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于离子反应:M2O7x-+3S2﹣+14H+=2M3++3S↓+7H2O其中x值和M2O7x-离子中M化合价分别是______和______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com