
| A、说明AgCl没有完全电离,AgCl是弱电解质 |
| B、明溶解的AgCl已完全电离,AgCl是强电解质 |
| C、说明Ag+与Cl-的反应不能完全进行到底 |
| D、说明Ag+与Cl-的反应可以完全进行到底 |
科目:高中化学 来源: 题型:
| A、等压时,通入惰性气体,C的物质的量增大 |
| B、等压时,通入X气体,反应器中温度不变 |
| C、等容时,通入惰性气体,各反应速率不变 |
| D、等容时,通入X气体,Y的物质的量浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
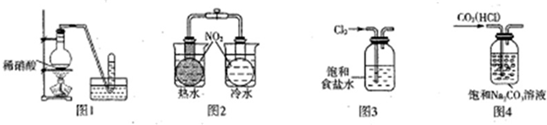
| A、图l用于制取纯净的NO2气体 |
| B、图2用于研究温度对化学平衡的影响 |
| C、图3用于实验室Cl2的收集 |
| D、图4用于除去CO2气体中的HCl杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
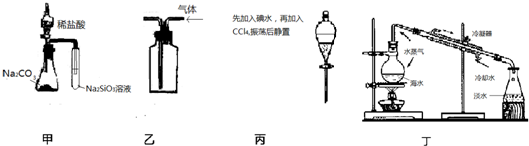
| A、用装置甲所示实验可比较氯、碳、硅三种元素的非金属性强弱 |
| B、用图乙所示实验装置排空气法收集CH4气体 |
| C、用装置丙萃取碘水中的碘 |
| D、用装置丁进行海水蒸馏得淡水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Cl-、CO32-、SO32- |
| B、K+、ClO-、Cl-、SO42- |
| C、Ca2+、Mg2+、NO3-、HCO3- |
| D、NH4+、Ba2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在密闭容器中加入1mol N2和3mol H2,充分反应生成NH3分子数为2NA |
| B、标准状况下,22.4L的CCl4分子中含有共价键数为4NA |
| C、常温常压下,1mol NaHSO4晶体中含有2NA个离子 |
| D、电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数一定为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com