
ЎҫМвДҝЎҝ
ТФУР»ъОпA әПіЙҫЫхҘАаёЯ·ЦЧУ»ҜәПОпF өДВ·ПЯИзПВ:

ТСЦӘ: 
(1) AЙъіЙB өД·ҙУҰАаРНОӘ_________Ј¬C ЦР№ЩДЬНЕөДГыіЖОӘ__________ ЎЈ
(2) D УлNaOH Л®ИЬТә·ҙУҰөД»ҜС§·ҪіМКҪОӘ__________ ЎЈ
(3) ўЩE ЙъіЙF өД»ҜС§·ҪіМКҪОӘ__________ЎЈ
ўЪИфFөДЖҪҫщПа¶Ф·ЦЧУЦКБҝОӘ20000Ј¬ФтЖдЖҪҫщҫЫәП¶ИОӘ________ (МоСЎПоЧЦДё)ЎЈ
A.54 B.108 C.119 D.133
(4) E ФЪТ»¶ЁМхјюПВ»№ҝЙТФәПіЙә¬УРБщФӘ»·Ҫб№№өДGЈ¬G өДҪб№№јтКҪОӘ__________ЎЈ
(5) ВъЧгПВБРМхјюөДC өДН¬·ЦТм№№МеУР___ЦЦ(І»ҝјВЗБўМеТм№№)ЎЈ
ўЩә¬УР1ёцБщФӘМј»·Ј¬ЗТ»·ЙППаБЪ4 ёцМјФӯЧУЙПёчБ¬УРТ»ёцИЎҙъ»щ
ўЪ1mol ёГОпЦКУлРВЦЖЗвСх»ҜНӯРьЧЗТә·ҙУҰІъЙъ2mol Ч©әмЙ«іБөн
(6) РҙіцТФ![]() ОӘФӯБП(ЖдЛыКФјБИОСЎ) ЦЖұё»ҜәПОп
ОӘФӯБП(ЖдЛыКФјБИОСЎ) ЦЖұё»ҜәПОп өДәПіЙВ·ПЯЈ¬ЗлУГТФПВ·ҪКҪұнКҫ:
өДәПіЙВ·ПЯЈ¬ЗлУГТФПВ·ҪКҪұнКҫ:  ЎЈ___________________ЎЈ
ЎЈ___________________ЎЈ
Ўҫҙр°ёЎҝ Сх»Ҝ·ҙУҰ МјМјЛ«јьЎўхҘ»щ 
 C
C  12
12 
ЎҫҪвОцЎҝёщҫЭCөДҪб№№әНBЎъCөДМхјюҝЙЦӘЈ¬BОӘЛбЈ¬BөДҪб№№јтКҪОӘ Ј¬ёщҫЭРЕПўЈ¬CУлде»ҜЗвјУіЙЙъіЙDЈ¬DОӘ
Ј¬ёщҫЭРЕПўЈ¬CУлде»ҜЗвјУіЙЙъіЙDЈ¬DОӘ Ј¬DФЪЗвСх»ҜДЖИЬТәЦРЛ®ҪвәуЛб»ҜЙъіЙEЈ¬EОӘ
Ј¬DФЪЗвСх»ҜДЖИЬТәЦРЛ®ҪвәуЛб»ҜЙъіЙEЈ¬EОӘ Ј¬Т»¶ЁМхјюПВE·ўЙъ·ЦЧУјдөДхҘ»Ҝ·ҙУҰЙъіЙёЯ·ЦЧУ»ҜәПОпFЈ¬FОӘ
Ј¬Т»¶ЁМхјюПВE·ўЙъ·ЦЧУјдөДхҘ»Ҝ·ҙУҰЙъіЙёЯ·ЦЧУ»ҜәПОпFЈ¬FОӘ ЎЈ
ЎЈ
(1)ёщҫЭЙПКц·ЦОцЈ¬AЦРөДИ©»щСх»ҜЙъіЙBЦРөДфИ»щЈ¬CЦР№ЩДЬНЕУРМјМјЛ«јьЎўхҘ»щЈ¬№Кҙр°ёОӘЈәСх»Ҝ·ҙУҰЈ»МјМјЛ«јьЎўхҘ»щЈ»
(2)D( )УлNaOHЛ®ИЬТә·ҙУҰөД»ҜС§·ҪіМКҪОӘ
)УлNaOHЛ®ИЬТә·ҙУҰөД»ҜС§·ҪіМКҪОӘ Ј¬№Кҙр°ёОӘЈә
Ј¬№Кҙр°ёОӘЈә Ј»
Ј»
(3)ўЩТ»¶ЁМхјюПВE·ўЙъ·ЦЧУјдөДхҘ»Ҝ·ҙУҰЙъіЙёЯ·ЦЧУ»ҜәПОпF Ј¬·ҙУҰөД»ҜС§·ҪіМКҪОӘ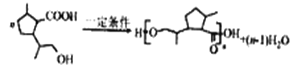 Ј¬№Кҙр°ёОӘЈә
Ј¬№Кҙр°ёОӘЈә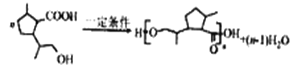 Ј»
Ј»
ўЪFөДБҙҪЪөДКҪБҝОӘ168Ј¬ИфFөДЖҪҫщПа¶Ф·ЦЧУЦКБҝОӘ20000Ј¬ФтЖдЖҪҫщҫЫәП¶Иn=![]() =118.9Ј¬№КСЎCЈ»
=118.9Ј¬№КСЎCЈ»
(4)E( )ФЪТ»¶ЁМхјюПВ»№ҝЙТФ·ЦЧУДЪ·ўЙъхҘ»Ҝ·ҙУҰЙъіЙә¬УРБщФӘ»·Ҫб№№өДGЈ¬ФтGөДҪб№№јтКҪОӘ
)ФЪТ»¶ЁМхјюПВ»№ҝЙТФ·ЦЧУДЪ·ўЙъхҘ»Ҝ·ҙУҰЙъіЙә¬УРБщФӘ»·Ҫб№№өДGЈ¬ФтGөДҪб№№јтКҪОӘ Ј¬№Кҙр°ёОӘЈә
Ј¬№Кҙр°ёОӘЈә Ј»
Ј»
(5)CОӘ Ј¬ўЩә¬УР1ёцБщФӘМј»·Ј¬ЗТ»·ЙППаБЪ4ёцМјФӯЧУЙПёчБ¬УРТ»ёцИЎҙъ»щ
Ј¬ўЩә¬УР1ёцБщФӘМј»·Ј¬ЗТ»·ЙППаБЪ4ёцМјФӯЧУЙПёчБ¬УРТ»ёцИЎҙъ»щ
ўЪ1molёГОпЦКУлРВЦЖЗвСх»ҜНӯРьЧЗТә·ҙУҰІъЙъ2molЧ©әмЙ«іБөнЈ¬ЛөГч·ЦЧУЦРә¬УР2ёцИ©»щЈ¬Фт»·ЙПЦ»ә¬УРМјМјөҘјьЈ¬ВъЧгМхјюөДҪб№№УРЈәБщФӘМј»·ЙПә¬УР1ёцјЧ»щЎў2ёцИ©»щәН1ёцТТ»щөДУР6ЦЦЈ»БщФӘМј»·ЙПә¬УР2ёцјЧ»щЎў1ёцИ©»щәН1ёцЎӘCH2CHOөДУР6ЦЦЈ»№І12ЦЦЈ¬№Кҙр°ёОӘЈә12Ј»
(6)ТФ![]() ОӘФӯБПЦЖұё»ҜәПОп
ОӘФӯБПЦЖұё»ҜәПОп Ј¬ҝЙТФКЧПИҪ«
Ј¬ҝЙТФКЧПИҪ« Л®ҪвОӘ
Л®ҪвОӘ![]() Ј¬¶шТӘәПіЙ
Ј¬¶шТӘәПіЙ![]() Ј¬фИ»щҝЙТФУЙИ©»щСх»ҜөГөҪЈ¬ТэИлфЗ»щҝЙТФКЧПИФЪМјМјЛ«јьЙПТэИлдеФӯЧУЈ¬ФЩЛ®ҪвЈ¬ёщҫЭМвёЙБчіМНјЈ¬ҪбәП·ҙУҰМхјю¶Ф№ЩДЬНЕөДУ°ПмЈ¬әПіЙВ·ПЯОӘ
Ј¬фИ»щҝЙТФУЙИ©»щСх»ҜөГөҪЈ¬ТэИлфЗ»щҝЙТФКЧПИФЪМјМјЛ«јьЙПТэИлдеФӯЧУЈ¬ФЩЛ®ҪвЈ¬ёщҫЭМвёЙБчіМНјЈ¬ҪбәП·ҙУҰМхјю¶Ф№ЩДЬНЕөДУ°ПмЈ¬әПіЙВ·ПЯОӘ Ј¬№Кҙр°ёОӘЈә
Ј¬№Кҙр°ёОӘЈә ЎЈ
ЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРИЬТәТ»¶ЁПФЛбРФөДКЗЈЁ Ј©
A.pHЈј7өДИЬТә
B.cЈЁH+Ј©ЈҫcЈЁOH©ҒЈ© өДИЬТә
C.cЈЁH+Ј©=1ЎБ10©Ғ7molL©Ғ1
D.cЈЁH+Ј©=cЈЁOH©ҒЈ© өДИЬТә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝКөСйКТҙУёЙәЈҙшЦРМбИЎөвөДІЩЧч№эіМЦРЈ¬ТЗЖчСЎУГҙнОуөДКЗ( )
A.іЖИЎТ»¶ЁЦКБҝөДёЙәЈҙшЎӘЎӘНРЕММмЖҪ
B.ЧЖЙХёЙәЈҙшЦБНкИ«ұдіЙ»ТҪэЎӘЎӘХф·ўГу
C.№эВЛәЈҙш»ТЛ®»мәПОпЎӘЎӘВ©¶·
D.ФЪәЈҙш»ТҪюИЎТәЦРјУИлККБҝВИЛ®әуЈ¬УГЛДВИ»ҜМјМбИЎөвЎӘЎӘ·ЦТәВ©¶·
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘЈә2CO(g)Ј«O2(g)===2CO2(g)ЎЎҰӨHЈҪЈӯ566 kJЎӨmolЈӯ1
Na2O2(s)Ј«CO2(g)===Na2CO3(s)Ј«![]() O2(g)ЎЎҰӨHЈҪЈӯ266 kJЎӨmolЈӯ1
O2(g)ЎЎҰӨHЈҪЈӯ266 kJЎӨmolЈӯ1
ёщҫЭТФЙПИИ»ҜС§·ҪіМКҪЕР¶ПЈ¬ПВБРЛө·ЁХэИ·өДКЗ(ЎЎЎЎ)
A. COөДИјЙХИИОӘ283 kJ
B. УТНјҝЙұнКҫУЙCOЙъіЙCO2өД·ҙУҰ№эіМәНДЬБҝ№ШПө
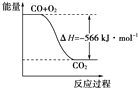
C. 2Na2O2(s)Ј«2CO2(s)===2Na2CO3(s)Ј«O2(g)ЎЎҰӨH > Јӯ532 kJЎӨmolЈӯ1
D. CO(g)УлNa2O2(s)·ҙУҰ·Еіц549 kJИИБҝКұЈ¬өзЧУЧӘТЖКэОӘ6.02ЎБ1023
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР·ҙУҰјИКЗСх»Ҝ»№Фӯ·ҙУҰ,УЦКЗ·ЕИИ·ҙУҰөДКЗ( )
A.Ba(OH)2ЎӨ8H2OУлNH4ClөД·ҙУҰB.ВБУлПЎСОЛбөД·ҙУҰ
C.ЧЖИИөДМјУл¶юСх»ҜМјөД·ҙУҰD.ЗвСх»ҜДЖУлСОЛбөД·ҙУҰ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝWЎўXЎўYЎўZКЗЛДЦЦіЈјыөД¶МЦЬЖЪФӘЛШ,ЖдФӯЧУ°лҫ¶ЛжФӯЧУРтКэұд»ҜИзНјЛщКҫ.ТСЦӘWөДТ»ЦЦәЛЛШөДЦКБҝКэОӘ18,ЦРЧУКэОӘ10;XәНNeФӯЧУөДәЛНвөзЧУКэПаІо1;YөДөҘЦККЗТ»ЦЦіЈјыөД°лөјМеІДБП;ZөД·ЗҪрКфРФФЪН¬ЦЬЖЪЦчЧеФӘЛШЦРЧоЗҝ.ПВБРұнКцЦРХэИ·өДКЗЈЁ Ј©
A. XО»УЪФӘЛШЦЬЖЪұнЦРөЪ¶юЦЬЖЪөЪIAЧе
B. XөДөҘЦКәНYөДөҘЦКПаұИ,ИЫөгҪПёЯөДКЗX
C. ZөДСх»ҜОпөДЛ®»ҜОпТ»¶ЁКЗЗҝЛб
D. WЎўXҝЙРОіЙX2WЎўX2W2АлЧУ»ҜәПОпЈ¬ЗТТхСфАлЧУёцКэұИҫщОӘ1:2
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјЛщКҫЈ¬јЧіШөДЧЬ·ҙУҰКҪОӘЈә ![]() Ј¬ПВБР№ШУЪёГөзіШ№ӨЧчКұөДЛө·ЁХэИ·өДКЗ
Ј¬ПВБР№ШУЪёГөзіШ№ӨЧчКұөДЛө·ЁХэИ·өДКЗ![]()
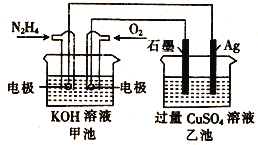
A. ёГЧ°ЦГ№ӨЧчКұЈ¬Agөзј«ЙПУРЖшМеЙъіЙ
B. јЧіШЦРёәј«·ҙУҰОӘ![]()
C. јЧіШәНТТіШЦРөДИЬТәөДpHҫщјхРЎ
D. өұјЧіШЦРПыәД![]()
![]() КұЈ¬ТТіШЦРАнВЫЙПЧо¶аІъЙъ
КұЈ¬ТТіШЦРАнВЫЙПЧо¶аІъЙъ![]() №ММе
№ММе
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТ»¶ЁОВ¶ИПВЈ¬ФЪ3ёцМе»эҫщОӘ1.0LөДәгИЭГЬұХИЭЖчЦР·ҙУҰ2SO2(g)+O2(g)![]() 2SO3(g)ҙпөҪЖҪәвЎЈПВБРЛө·ЁХэИ·өДКЗ
2SO3(g)ҙпөҪЖҪәвЎЈПВБРЛө·ЁХэИ·өДКЗ
ИЭЖч | ОВ¶И/K | ОпЦКөДЖрКјЕЁ¶И/mol/L | ОпЦКөДЖҪәвЕЁ¶И/mol/L | SO2»тSO3ЖҪәвЧӘ»ҜВК | ||
c(SO2) | c(O2) | c(SO3) | cЈЁSO3Ј© | |||
I | 723 | 0.2 | 0.1 | 0 | 0.16 | a1 |
II | 723 | 0.4 | 0.2 | 0 | a2 | |
III | 823 | 0 | 0 | 0.2 | a3 | |
A. ҙпөҪЖҪәвКұЈ¬a1+a3>1
B. ҙпөҪЖҪәвКұЈ¬ИЭЖчЦРөДС№Зҝ: PII>PI>PIII
C. ҙпөҪЖҪәвКұЈ¬ИЭЖчIIIЦРөДДж·ҙУҰЛЩВКұИИЭЖчIЦРөДҙу
D. ИфЖрКјКұЈ¬ПтИЭЖчIЦРідИл0.16molSO2Ўў0.04molO2әН0.16molSO3Ј¬ФтҙЛКұ·ҙУҰПтДж·ҙУҰ·ҪПтҪшРР
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com