
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。正极电极反应为__________。
(2)某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为 ________,当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是_________。
(3)燃料电池是一种高效、环境友好的供电装置,如下图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①该电池的正极反应式__________________________。
②若该电池的效率80%,当外电路通过0.2mo1电子时,消耗O2的体积____L(标准状况)
【答案】PbO2+4H++SO42-+2e-=PbSO4+2H2O Cu-2e=Cu2+ 0.05NA O2+4e-+4H+=2H2O 1.4
【解析】
(1)根据铅蓄电池中正极得到电子发生还原反应生成硫酸铅,写出电极方程式;
(2)根据总反应可知铜发生氧化反应,则铜失电子作原电池的负极;Ag为原电池的正极,正极上发生还原反应,根据电极反应式计算转移电子的数目;
(3)氢氧燃料电池中,通入氧气的一极为正极,发生还原反应;根据原电池中得失电子数目相等进行计算。
(1)铅蓄电池的电池总反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,依据反应的总电池反应,反应中PbO2中元素化合价降低的是在正极得到电子发生还原反应生成硫酸铅,电极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O;故答案为:PbO2+2e-+4H++SO42-=PbSO4+2H2O。
(2)在2Ag++Cu═Cu2++2Ag反应中,铜的化合价升高,发生氧化反应,则铜失电子作原电池的负极,电极反应为Cu-2e-═Cu2+;原电池工作时,负极铜失去电子被氧化生成铜离子,铜的质量逐渐减少,溶液中的银离子在正极银得电子发生还原反应生成银,所以正极增重的质量就是析出银的质量,当银电极质量增加5.4g时,n(Ag)=5.4g÷108g/mol =0.05mol,根据电极反应Ag++e-=Ag,可知原电池反应共转移电子的数目为0.05NA,故答案为:Cu-2e-═Cu2+;0.05NA。
(3)①氢氧燃料电池中,通入氧气的一极为正极,发生还原反应,该电池的正极方程式为:O2+4e-+4H+=2H2O;故答案为:O2+4e-+4H+=2H2O。
②设参加反应的氧气的体积为VL(标准状况),则![]() ×80%×4mol=0.2mol,解得V=1.4L,故答案为:1.4。
×80%×4mol=0.2mol,解得V=1.4L,故答案为:1.4。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 1 mol乙烷和1 mol乙烯中,化学键数相同
C. 1 mol D2O与1 mol H2O中,中子数比为2∶1
D. 同等质量的氧气和臭氧中,电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据下图中数据填空:

(1)平衡时容器内混合气体密度比起始时_____(填“变大”,“变小”或“相等”下同),混合气体的平均相对分子质量比起始时_____;
(2)将amolX与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=_____。
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强 ②混合气体的密度 ③混合气体的总物质的量 ④混合气体的平均相对分子质量 ⑤混合气体的颜色 ⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(1)一定能证明2SO2(g)+O2(g)![]() 2SO3(g)达到平衡状态的是_____(填序号,下同)。
2SO3(g)达到平衡状态的是_____(填序号,下同)。
(2)一定能证明I2(g)+H2(g)![]() 2HI(g)达到平衡状态的是______。
2HI(g)达到平衡状态的是______。
(3)一定能证明A(s)+2B(g)![]() C(g)+D(g)达到平衡状态的是_____。(注:B,C,D均为无色物质)
C(g)+D(g)达到平衡状态的是_____。(注:B,C,D均为无色物质)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型及分子结构示意图如下:

(1)下列有关石墨烯说法正确的是________。
A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12 g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①钴原子在基态时,核外电子排布式为________。
②乙醇沸点比氯乙烷高,主要原因是_______________________。
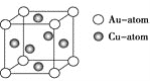
③下图是金与铜形成的金属互化物合金,它的化学式可表示为:________。
④含碳原子且属于非极性分子的是________;
a.甲烷 b.乙炔 c.苯 d.乙醇
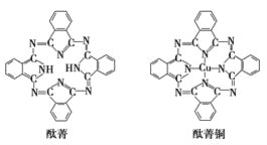
⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH- ![]() CH3COONH4 +3NH3+2Ag↓+H2O
CH3COONH4 +3NH3+2Ag↓+H2O
B. 苯酚钠溶液中通入少量CO2:CO2 +H2O+2C6H5O-→2C6H5OH+CO32-
C. 氯乙烷中滴入AgNO3溶液检验其中氯元素:Cl-+Ag+=AgCl↓
D. 乙酸滴入氢氧化铜悬浊液中:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
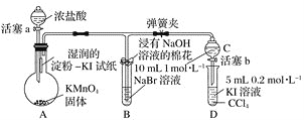
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的离子方程式是____________________________________________。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是____________________________。
(4)过程Ⅲ实验的目的是________________________________________________________。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐________,得电子能力逐渐________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的一组是( )
①糖类、油脂、蛋白质在一定条件下都能发生水解
②制造婴儿用的一次性纸尿片采用的吸水保水的材料可以是![]()
③石油的分馏、裂化和煤的干馏都是化学变化
④葡萄糖与果糖、淀粉与纤维素均互为同分异构体
⑤淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应
⑥塑料、橡胶和纤维都是合成高分子材料
⑦向蛋白质溶液中加入饱和CuSO4溶液,出现盐析现象,加水溶解
A. ②⑤ B. ①⑤⑦ C. ③④⑥ D. ②⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活水平的不断提高和环境保护意识的不断增强,家庭绿化日益普及。对绿色观叶植物适当补充镁元素,可使其正常生长,其原因是( )
A. 镁是合成蛋白质的原料
B. 镁是合成核酸的原料
C. 镁能够促进植物对水分的吸收
D. 镁是组成叶绿素的重要元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com