
分析 根据核内质子数=核外核外电子数-电荷数,中子数=质量数-质子数,计算X原子中子数,进而计算每个DmX分子含有中子数,根据n=$\frac{m}{M}$计算DmX的物质的量,结合每个分子含有中子数计算.
解答 解:某元素的一种同位素离子Xm-的质量数为A,核内质子数=b-m,则中子数为(A-b+m),则每个DmX分子含有中子数为(A-b+m+m),ag HmX的物质的量为$\frac{ag}{(A+2m)g/mol}$=$\frac{a}{A+2m}$mol,故含有中子物质的量为$\frac{a}{A+2m}$(A-b+2m)mol;
故答案为:$\frac{a}{A+2m}$(A-b+2m).
点评 本题主要考查了质子数、中子数、质量数、核外电子数之间的关系,难度不大,把握阴离子中核外电子数的计算方法是解题的关键.


科目:高中化学 来源: 题型:解答题

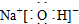 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烷 | B. | 一定有丙烷 | ||
| C. | 可能是乙烷和丙烷的混合物 | D. | 可能是甲烷和丁烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
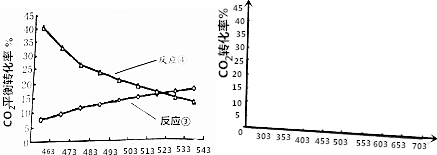
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
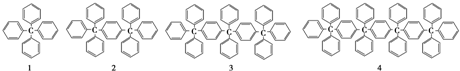
| A. | C158H118 | B. | C158H116 | C. | C160H116 | D. | C160H118 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | C | |
| B |
| A. | A、B、C三元素的气态氢化物溶于水均显酸性 | |
| B. | A、B两种元素的气态氢化物均能与它们的最高价氧化物对应的水化物发生反应,且反应类型相同 | |
| C. | C在周期表中的位置为第二周期第ⅦA族,最高价为+7价 | |
| D. | B02是酸性氧化物,AO2不是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 6.4g铜与足量的硫磺在绝隔空气的条件下反应,电子转移的数目为0.1NA | |
| D. | 1mol白磷分子中所含共价键数为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com