
| A. | 150ml 0.2mol/L NaCl溶液 | B. | 100ml 3mol/L NH4Cl溶液 | ||
| C. | 300ml 0.1mol/L KCl溶液 | D. | 150ml 0.1mol/L FeCl3溶液 |
分析 根据离子的物质的量浓度=溶质的物质的量浓度×溶质中含有离子的个数,与溶液的体积无关来分析.
解答 解:A、150mL 0.2mol•L-1的NaCl溶液中Cl-浓度为0.2mol•L-1×1=0.2mol•L-1;
B、100mL 3mol•L-1NH4Cl溶液中Cl-浓度为3mol•L-1×1=3mol•L-1;
C、300 mL 0.1mol•L-1的KCl溶液中Cl-浓度为0.1mol•L-1×1=0.1mol•L-1;
D、150mL 0.1 mol•L-1的FeCl3溶液中Cl-浓度为0.1mol•L-1×3=0.3mol•L-1;
故选D.
点评 本题考查了物质的量浓度的计算,难度较小,明确物质的构成是解答本题的关键,并注意离子的浓度与溶液的浓度的关系来解答即可.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学研究会造成严重的环境污染,最终人类会毁灭在化学物质中 | |
| B. | 化学研究的主要目的是认识分子 | |
| C. | 化学家可以制造出自然界中不存在的物质 | |
| D. | 俄国化学家门捷列夫提出了原子学说,为近代化学的发展奠定了基础 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 离子半径:C>D>A>B | B. | 核电核数:b>a>d>c | ||
| C. | 原子半径:A>B>D>C | D. | 元素的电负性:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当10NA个电子转移时,该反应放出1300 kJ的能量 | |
| B. | 当1NA个水分子生成且为液体时,吸收1300 kJ的能量 | |
| C. | 当2NA个碳氧共用电子对生成时,放出1300 kJ的能量 | |
| D. | 当8NA个碳氧共用电子对生成时,吸收1300 kJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++H2↑ | |
| B. | 大理石与盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 铜和硝酸银溶液反应:Cu+Ag+=Ca2++Ag | |
| D. | 硫酸与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L氧气中,一定含有2 mol氧原子 | |
| B. | 80 g NaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L | |
| C. | 18 g水在标准状况下的体积约为22.4 L | |
| D. | 标准状况下,20 mL NH3跟60 mL O2所含分子个数比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
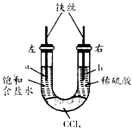 利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )
利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )| A. | 左管中O2得到电子,右管中H+得到电子 | |
| B. | 一段时间后,左管液面低于右管液面 | |
| C. | a、b两处具有相同的电极反应式:Fe-3e-=Fe3+ | |
| D. | a处溶液的pH增大,b处溶液的pH减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com