
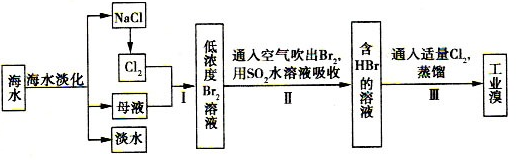
 MgO+2HCl↑+5H2O
MgO+2HCl↑+5H2O

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
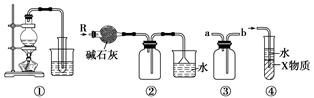
| A.装置①可制取少量蒸馏水 |
| B.装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C.装置③可用于排空气法收集H2、CO2、Cl2、HCl、NO等气体 |
| D.装置④中X物质若为四氯化碳,则可用于吸收氨气或氯化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
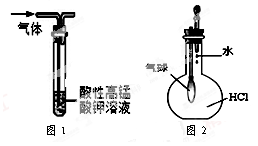
| A.用干燥pH试纸测定某新制氯水的pH |
| B.用图1装置能除去SO2中混有的CO2 |
| C.用图2装置能验证HCl气体在水中的溶解性 |
| D.用25 mL碱式滴定管量取20.00 mLKMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
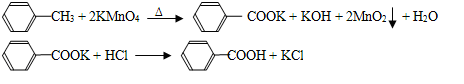
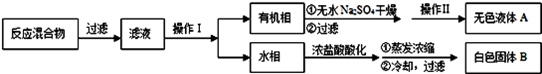
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中, 加热溶解, | 得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中, | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, | | 白色晶体是苯甲酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | A | B | C | D |
| 装置 | 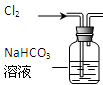 | 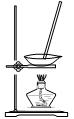 | 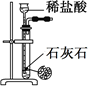 |  |
| 目的 | 除去Cl2中含有的少量HCl | 蒸干NH4Cl饱和溶液制备NH4Cl晶体 | 制取少量纯净的CO2气体 | 分离CCl4萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
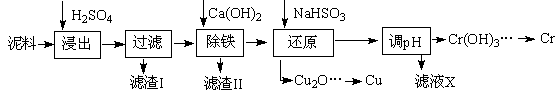
| | Fe3+ | Cu2+ | Cr3+ |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
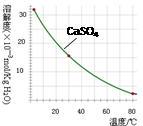
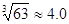 )
)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Ca2++2K++Mg2++4
2Ca2++2K++Mg2++4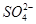 +2H2O
+2H2O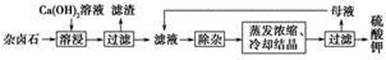
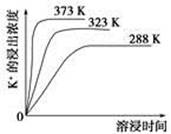
 ?
? CaCO3(s)+
CaCO3(s)+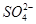
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入AgNO3溶液有白色沉淀产生 |
| B.加入稀盐酸有无色无味气体产生,该气体可使澄清的石灰水变浑浊 |
| C.加入MgCl2溶液有白色沉淀产生,再加入稀盐酸沉淀溶解,并产生可使澄清石灰水变浑浊的无色无味气体 |
| D.加入Ba(OH)2溶液有白色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将某气体通入品红溶液中,品红褪色,说明该气体一定是SO2 |
| B.用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明该溶液一定不存在K+ |
| C.利用一束强光照射明矾溶液,产生光亮的“通路”,说明明矾一定发生了水解 |
| D.向含X的溶液中加入银氨溶液,水浴加热,无银镜现象,说明X中一定不含醛基 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com