
A.Na2S 的电子式: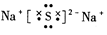 | B.Clˉ的结构示意图: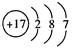 |
| C.I—131 : 78 53I | D.乙烯的结构式:CH2=CH2 |
科目:高中化学 来源:不详 题型:单选题
| A.KCl中含有35Cl | B.KCl中含有37Cl |
| C.生成物Cl2的相对分子质量大于71 | D.该反应转移的电子数为6e- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | | | | | ① | | ② | |
| 三 | ③ | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验事实 | 结 论 |
| ① | A元素的原子半径比B元素的原子半径大 | 周期表中A位于B的下一周期 |
| ② | 将CO2通入到Na2SiO3溶液中产生白色浑浊(H2SiO3) | 酸性: H2CO3>H2SiO3 |
| ③ | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色溶液中加入硝酸酸化的硝酸钡溶液产生白色沉淀 | 原溶液一定有SO42- |
| A.③④⑤ | B.①②③⑤ | C.②③ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
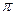 键。
键。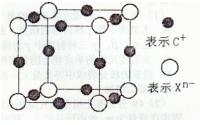
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱金属单质在化学反应中表现出强还原性 |
| B.Li 在氧气中燃烧主要生成Li2O2 |
| C.碱金属离子的氧化性随着离子半径的增大而减小 |
| D.随核电荷数的增加,单质与水反应剧烈程度增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.发生化学反应时,失去电子越多的金属原子,其还原能力越强 |
| B.目前已发现113种元素,即已发现113种原子 |
| C.核外电子总数不同的原子,可能是同种元素的原子 |
| D.同一元素的各种同位素的化学性质基本相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com