
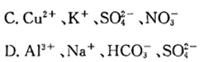
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.常温下,c(H+)/c(OH-)=1010的溶液:Fe2+、K+、NO3-、SO42- |
| B.加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42- |
| C.加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2- |
| D.由水电离产生的c(H+)=1×10—12的溶液:NH4+、Na+、AlO2-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.在饱和氯水中 Cl-、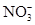 、Na+、 、Na+、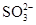 可以大量共存 可以大量共存 |
| B.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| C.向无色溶液中滴加氯水和CCl4,振荡、静置下层溶液显紫色说明原溶液中有I― |
D.SO2通入碘水中,反应的离子方程式为SO2+I2+H2O= 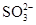 +2I―+2H+ +2I―+2H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑤ | B.②⑤⑥ | C.①②⑥ | D.③④⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.空气 SO2、NO、NO2 |
| B.KNO3溶液 Fe2+、H+、I- |
| C.NaHCO3溶液 Ca2+、OH-、Cl- |
| D.由水电离产生的c(H+) = 10-11mol·L-1的溶液 K+、SO42-、Br- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg2+、NO3-、Cl-、Na+ | B.Al3+、SO42-、Cl-、K+ |
| C.Na+、Fe2+、SO42-、NO3- | D.S2-、SO32-、K+、Na+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定不存在Ba2+,可能存在NH4+ |
| B.不可能存在Ba2+、Cl- |
| C.Na+一定存在,且c(Na+)≥0.2 mol/L |
| D.Na+、Cl-可能存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Mg2+、Fe3+、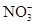 、SCN- 、SCN- | B.Al3+、Fe2+、Cl-、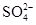 |
C.K+、Na+、Cl-、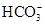 | D.Na+、Ba2+、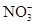 、 、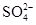 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com