

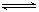 XeF4(g)+F2(g),
XeF4(g)+F2(g), 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
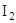 在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡: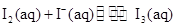 ,某
,某
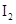 、KI混合溶液中,
、KI混合溶液中,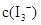 与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是
与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是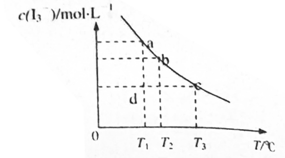
A.反应 |
B.状态a与状态b相比,状态b时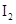 的转化率更高 的转化率更高 |
C.若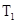 时,反应进行到状态d时,一定有 时,反应进行到状态d时,一定有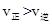 |
D.温度为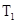 时,向该平衡体系中加入KI固体,平衡正向移动 时,向该平衡体系中加入KI固体,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得
2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得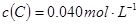 ,放出热量Q1 kJ。
,放出热量Q1 kJ。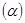 与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A)______________K(B)(填“>”、“<”或“=”)
与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A)______________K(B)(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
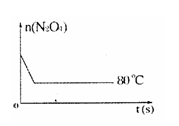
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
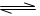 CH3OH(g)+H2O(g) △H = —49.0kJ/mo1.
CH3OH(g)+H2O(g) △H = —49.0kJ/mo1.
 mL与pH=11的NaOH溶液
mL与pH=11的NaOH溶液 mL混合反应而得,则下列说法中正确的是 __。
mL混合反应而得,则下列说法中正确的是 __。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
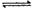 Fe(s)+CO2(g) △H=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) △H=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是| A.达到化学平衡状态时,若c (CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
| B.若要提高CO的转化率,则应该加入适当的过量FeO |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.若生成56 g Fe.则吸收的热量小于a kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
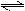 C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是
C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是| A.混合气体的密度不变 |
| B.A的消耗速率与D的生成速率相同 |
| C.单位时间内有1 mol A生成的同时,有1 mol C 消耗 |
| D.混合气体的相对分子质量不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2NO2 N2O4(正反应是放热反应) N2O4(正反应是放热反应) |
B.C(s)+CO2 2CO (正反应是吸热反应) 2CO (正反应是吸热反应) |
C.N2+3H2 2NH3(正反应是放热反应) 2NH3(正反应是放热反应) |
D.H2S H2+S(s)(正反应是吸热反应) H2+S(s)(正反应是吸热反应) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com