
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体。下列说法错误的是( )
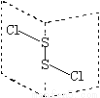
A.S2Cl2的结构中各原子均达到8电子的稳定结构
B.S2Cl2为含有极性键和非极性键的共价化合物
C.若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末考试化学试卷(解析版) 题型:选择题
化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是
A.垃圾是放错地方的资源,应分类回收利用
B.实现化石燃料清洁利用,就无需开发新能源
C.为提高农作物的产量和质量,应大量使用化肥和农药
D.将废弃的植物油(即“地沟油”)蒸馏可以重新作为食用油
查看答案和解析>>
科目:高中化学 来源:2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷(解析版) 题型:选择题
下列反应中,与其它三个反应不属于同一类型的反应是( )
A.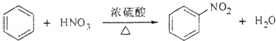
B.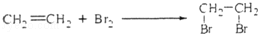
C.CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.CH4+Cl2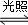 CH3Cl+HCl
CH3Cl+HCl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年中国石油天然气管道局中学高二下第二次月考化学试卷(解析版) 题型:推断题
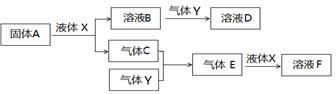
下表为元素周期表的一部分:
族 |
|
|
| |||||
1 | ① |
|
|
|
|
|
|
|
2 |
|
|
|
|
| ② |
|
|
3 | ③ |
|
| ④ |
| ⑤ | ⑥ |
|
I. 请参照元素①-⑥在表中的位置,用化学用语回答下列问题:
(1)画出元素②的离子结构示意图______________。
(2)②、③、⑤的离子半径由大到小的顺序为_________________________。
(3)元素④和⑥形成的化合物的电子式:____________________。
II. 由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答:
(4)写出固体A与液体X反应的离子方程式 。
(5)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,写出过量的Y与B
溶液反应的离子方程式__________________________________________________
(6)若气体C与Y在恒容绝热的条件下反应,下列哪些说法说明该反应达到平衡状态:_______
A. 温度不变
B. 2v正(C)=v逆(Y)
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年中国石油天然气管道局中学高二下第二次月考化学试卷(解析版) 题型:选择题
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
A. T1(OH)3是两性氢氧化物
B. 铊与酸反应比铝更剧烈
C. Tl3+的氧化能力比Al3+弱
D. 铊是易导电的银白色金属
查看答案和解析>>
科目:高中化学 来源:2015-2016学年中国石油天然气管道局中学高二下第二次月考化学试卷(解析版) 题型:选择题
用H2O2溶液处理含NaCN的废水的反应原理为:NaCN+H2O2+H2O===NaHCO3+NH3,已知:HCN
的酸性比H2CO3弱。下列有关说法正确的是( )
A.该反应中氮元素被氧化
B.该反应中H2O2作还原剂
C.0.1mol·L-1NaCN溶液中含有HCN和CN-的总数为0.1×6.02×1023
D.实验室配制NaCN溶液时,需加入适量的NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市十校联合体高二下学期期末联考化学试卷(解析版) 题型:填空题
硫代硫酸钠晶体(Na2S2O3·5H2O,式量248) 可用于照相行业的定影剂。它易溶于水,且溶解度随温度升高而显著增大,难溶于乙醇,加热时易分解,实验室模拟工业制备硫代硫酸钠晶体通常有两种方法。(硫单质不溶于水,微溶于酒精)
I 亚硫酸钠法:Na2SO3+S+5H2O=Na2S2O3·5H2O,简易实验流程如下:
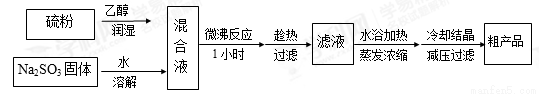
(1)硫粉用乙醇润湿的目的是 ;
(2)洗涤粗产品,下列洗涤剂最合适的是 ;
A.冰水 B.热水 C.乙醇 D.乙醇-水混合溶液
(3)所得粗产品一般通过 方法提纯;
II硫化碱法:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,主要实验装置如下:
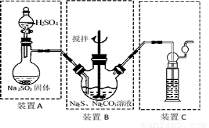
(4)装置C中可放入 ;
A.BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.NaOH溶液
(5)为测定粗产品中Na2S2O3•5H2O的纯度。某兴趣小组称取5.0 g粗产品配成250mL溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.01mol/L KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时到达滴定终点。实验数据如下表:
滴定次数 | 1 | 2 | 3 |
消耗Na2S2O3溶液(mL) | 19.98 | 21.18 | 20.02 |
该产品的纯度是 ;
(6)硫代硫酸钠产率受温度、pH影响如下图:
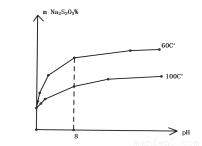
下列说法不正确的是 。
A.生成Na2S2O3一定是放热反应
B. 制备应采取较低温度
C.Na2S2O3一定能和0.1mol·L-1的硫酸发生反应
D.控制pH和温度,可以提高Na2S2O3的产率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市十校联合体高二下学期期末联考化学试卷(解析版) 题型:选择题
已知298K、101KPa条件下
2H2(g) + O2(g) = 2H2O(g) △H1= - 483.6kJ·mol-1
2H2(g) + O2(g) = 2H2O(l)△H2= - 571.6kJ·mol-1
据此判断,下列说法正确的是
A.H2(g)与O2(g)反应生成H2O(g)是吸热反应
B.1 molH2O(g)转变成1 molH2O(l)放出44.0kJ热量
C.1 molH2O(l)转变成1 molH2O(g)放出44.0kJ热量
D.1 molH2O(g)转变成1 molH2O(l)放出88.0kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com