
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2016-2017学年福建省、惠安一中、泉州实验中学高一上学期期末联考化学试卷(解析版) 题型:选择题
下列离子方程式中书写正确的是( )
A. 向FeCl2溶液中通入Cl2:Fe2+ + Cl2 = Fe3+ + 2Cl―
B. Ba(OH)2溶液与硫酸的反应:OH―+ H+ = H2O
C. 碳酸氢钠溶液与稀盐酸混合:HCO3―+ H+ = H2O+CO2↑
D. AlCl3溶液中加入过量氨水:Al3+ + 4OH― = AlO2― + 2H2O
查看答案和解析>>
科目:高中化学 来源:河南省南阳市2016-2017学年高二下学期第一次月考(3月)化学试卷 题型:选择题
下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
表述Ⅰ | 表述Ⅱ | |
A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1—与Na+间的作用力大于碘晶体中分子间的作用力 |
B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二开学质检(3月)化学试卷(解析版) 题型:简答题
(Ⅰ)(1)在25℃、101kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ。则甲醇的燃烧热的热化学方程式为:_________________________________
(Ⅱ)现用中和滴定测定某盐酸溶液的浓度,有关数据记录如下:
滴定序号 | 待测液体积(mL) | 所消耗烧碱标准液的体积(mL) | ||
滴定前 | 滴定后 | 消耗的体积 | ||
1 | 25.00 | 0.50 | 25.12 | 24.62 |
2 | 25.00 | / | / | / |
3 | 25.00 | 5.00 | 29.58 | 24.58 |
(2)实验中有石蕊和酚酞两种指示剂,该实验应选用_______作指示剂。用______式滴定管盛装0.2500 mol/L烧碱标准液,锥形瓶中装有25.00mL待测盐酸溶液。
(3)下图表示第二次滴定时50 mL滴定管中前后液面的位置。该次滴定所用标准烧碱溶液体积为_______mL。
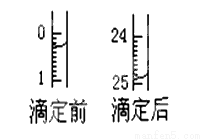
(4)根据所给数据,计算出该盐酸的物质的量浓度(注意保留合适的有效数字),c (HCl) = _____________ 。
(5)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果_________。(填“无影响”、“偏高”、“偏低”)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二开学质检(3月)化学试卷(解析版) 题型:选择题
已知0.1mol•L-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是( )
A. 在Na2A、NaHA两溶液中,离子种类不相同 B. 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
C. 在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等 D. 在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二开学质检(3月)化学试卷(解析版) 题型:选择题
下列叙述中正确的是( )
A. 化合反应一定是放热反应
B. 化学反应一定有物质变化,不一定有能量变化
C. 吸热反应不加热也可能发生
D. 放热反应不需要加热就一定能发生
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一(3月)开学质检化学试卷(解析版) 题型:选择题
下列各组物质中,X是主体物质,Y是少量杂质,Z是要除去杂质而加入的试剂,其中正确的组别是
X | Y | Z | |
A | FeCl2溶液 | FeCl3 | KSCN溶液 |
B | FeCl2溶液 | CuCl2 | Zn粉 |
C | Fe2(SO4)3溶液 | FeSO4 | C12 |
D | Fe粉 | A1粉 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三3月联考理科综合化学试卷(解析版) 题型:简答题
氟是自然界中广泛分布的元素之一。由于氟的特殊化学性质,它和其他卤素在单质及化合物的制备与性质上存在较明显的差异。
Ⅰ.化学家研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在 423 K 的温度下制备F2的化学方程式:_________________________。
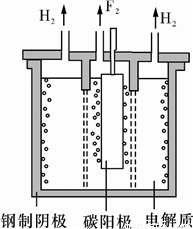
现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
已知KHF2是一种酸式盐,写出阴极上发生的电极反应式________________________。电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是___________。
Ⅱ.①卤化氢的熔沸点随相对分子质量增加而升高,而HF熔沸点高于HCl的原因是________________________。HF的水溶液是氢氟酸,能用于蚀刻玻璃,其化学反应方程式为:________________________
②已知25 ℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。
某pH=2的氢氟酸溶液,由水电离出的c(H+)=___________mol/L;若将0.01 mol/L HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度大小关系为:________________________。
③又已知25 ℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol/L HF溶液中加入 1 L 0.2 mol/L CaCl2 溶液,通过列式计算说明是否有沉淀产生:______________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列事实不能用元素周期律解释的只有( )
A. 碱性:KOH>NaOH
B. 相对原子质量:Ar>K
C. 酸性:HClO4>H2SO4
D. 元素的金属性:Mg>Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com