
| A. | 标准状况下,2.24L Cl2通入足量水中或NaOH溶液中,转移的电子数均为0.1NA. | |
| B. | 1mol CnH2n含有的共用电子对数为(3n+1)NA | |
| C. | 电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子书为0.2NA | |
| D. | 2gD2160中含中子、质子、电子数目均为NA |
分析 A、氯气和水的反应可逆反应;
B、CnH2n中含3n条共价键;
C、电解精炼铜时,阳极上放电的不止是铜,还有比铜活泼的金属;
D、求出重水的物质的量,然后根据1mol重水中含中子数、电子数和质子数均为10个来分析.
解答 解:A、氯气和水的反应可逆反应,不能进行彻底,故标况下2.24L即0.1mol氯气和水反应转移的电子数小于0.1NA个,故A错误;
B、CnH2n中含3n条共价键,故1mol中含共用电子对数为3nNA个,故B错误;
C、电解精炼铜时,阳极上放电的不止是铜,还有比铜活泼的金属,故当阳极质量减少6.4g时,转移的电子数大于0.2NA个,故C错误;
D、2g重水的物质的量为0.1mol,而1mol重水中含中子数、电子数和质子数均为10个,故0.1mol重水中含电子数、中子数和中子数均为NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期元素的正化合价由+1→+7依次升高 | |
| B. | PH3在空气中可以自燃,根据元素周期律可以推知SiH4很难燃烧 | |
| C. | Cl的非金属性强于S,所以HClO3的酸性一定强于H2SO3 | |
| D. | Li的电子层数小于Al,但是Li的原子半径却却大于Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
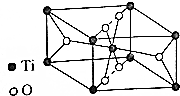 为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用.
为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用. ,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.
,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
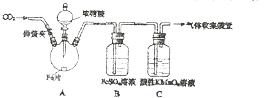 甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | / |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②③④⑤ | C. | ①②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| H | Z |
| A. | 常温下,含H的两种离子都能使水电离出的c•(H+)•c(OH-)增大 | |
| B. | Y的简单氢化物和Y的最高价含氧酸之间能发生氧化还原反应 | |
| C. | X的气态氢化物的热稳定性比Y的气态氢化物的热稳定性强 | |
| D. | 简单离子半径的大小顺序为H>Z>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com